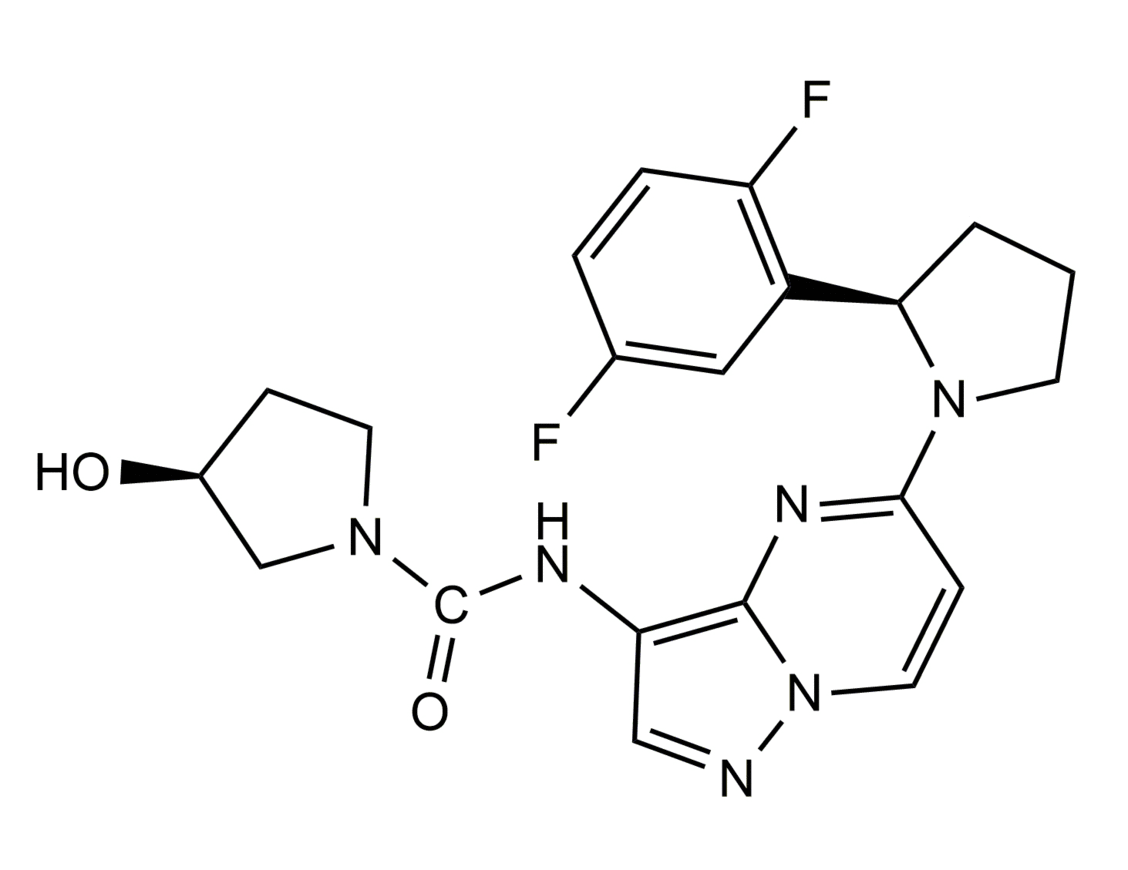
Tropomyosin-Rezeptorkinasen (TRK) sind an der Schmerz- und Thermoregulation sowie der Steuerung von Bewegung, Erinnerung, Appetit und des Metabolismus beteiligt. Es gibt drei Unterformen, TRKA, TRKB und TRKC, die von den neurotrophen TRK-Genen NTRK1, NTRK2 und NTRK3 kodiert werden. Ein NTRK-Gen kann zu einem Onkogen werden, wenn es mit einem anderen Gen fusioniert, wenn also beide Gene zerbrechen und sich anders als zuvor zusammenlagern. Das NTRK-Gen ist dann konstitutiv, also dauerhaft, aktiviert und das zugehörige TRK-Protein wird im Übermaß produziert.
Insgesamt sind NTRK-Fusionen selten; sie liegen über alle Tumorentitäten hinweg bei etwa 1 Prozent der Patienten vor. Bei manchen Krebsarten wie dem infantilen Fibrosarkom sind aber nahezu alle Patienten betroffen. Als Faustregel gilt, dass NTRK-Fusionen bei seltenen Tumoren häufig und bei häufigen Tumoren selten sind.