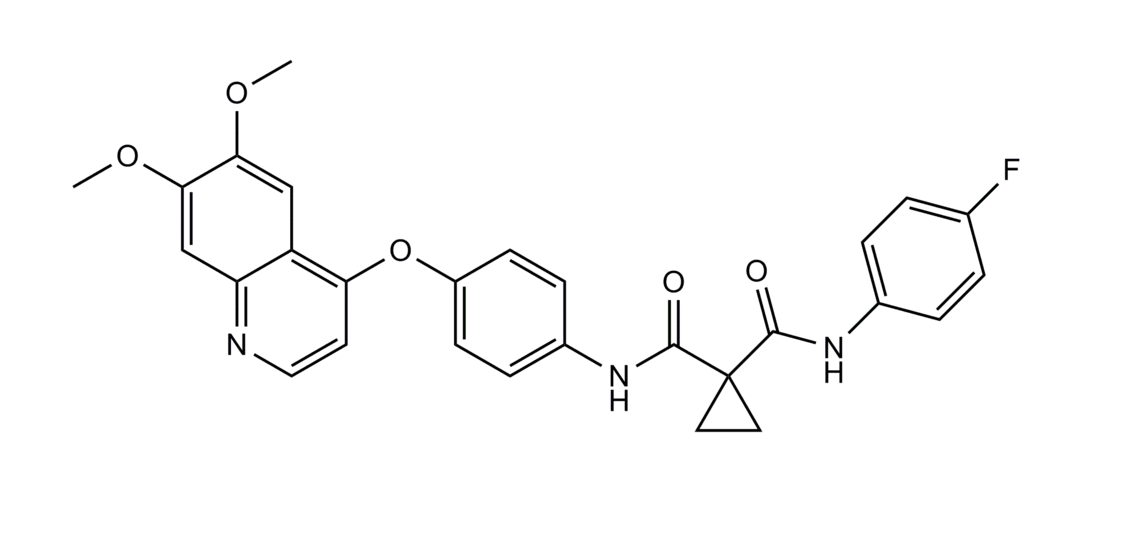
Sehr häufige Nebenwirkungen (bei mehr als 20 Prozent der Patienten) in Studien zu Cabozantinib waren Durchfall, Hand-Fuß-Syndrom (palmar-plantares Erythrodysästhesiesyndrom, das Hautausschlag und Taubheitsgefühl in den Handflächen und Fußsohlen beinhaltet), Gewichtsverlust, Appetitlosigkeit, Übelkeit, Müdigkeit, Geschmacksstörungen, Veränderungen der Haarfarbe, Hypertonie, Entzündungen der Schleimhaut einschließlich Stomatitis, Verstopfung, Erbrechen, Schwäche und Veränderungen im Klang der Stimme.
Sehr häufige schwerwiegende Nebenwirkungen sind Lungenentzündung, Schleimhautentzündung, Hypocalciämie, Dysphagie, Dehydratation, Lungenembolie und Hypertonie.
Die häufigsten Laborwert-Anomalien waren erhöhte Werte von Leberenzymen wie Aspartataminotransferase (AST), Alaninaminotransferase (ALT) und alkalischer Phosphatase (ALP), niedrige Zahlen der weißen Blutkörperchen (Lymphopenie oder Neutropenie), Thrombozytopenie, Hypocalciämie, Hypophosphatämie, Hypoalbuminämie und Hyperbilirubinämie.
Cabozantinib ist mit Erschöpfung und Schwäche assoziiert. Daher ist beim Führen eines Fahrzeugs oder beim Bedienen von Maschinen Vorsicht geboten.