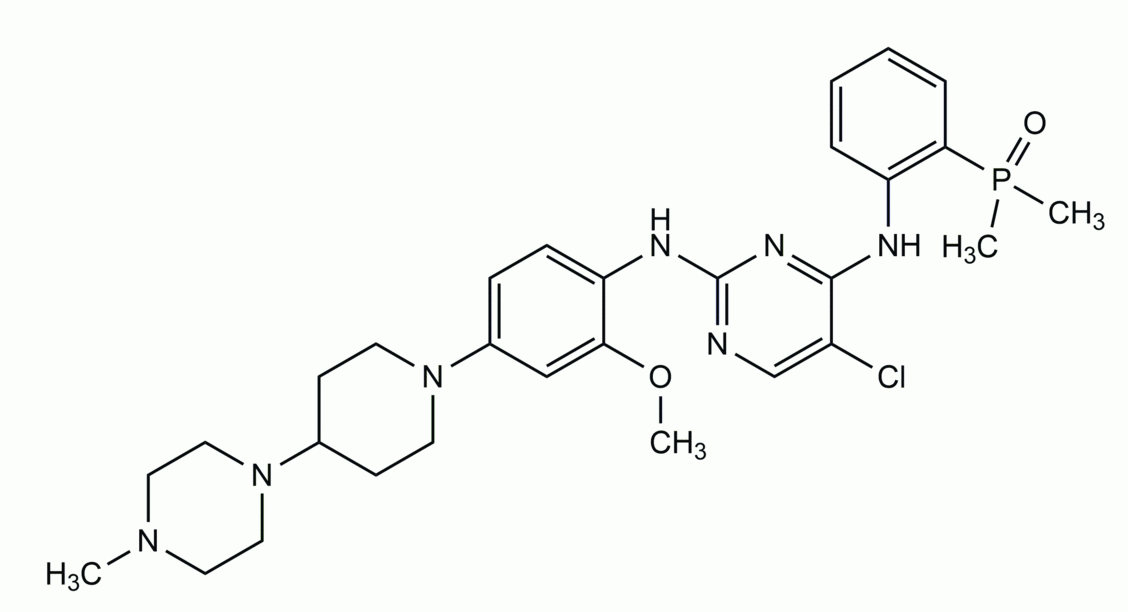
Sicherheit und Wirksamkeit von Brigatinib wurden in der randomisierten, offenen, multizentrischen Studie ALTA an 222 Patienten mit lokal fortgeschrittenem oder metastasiertem ALK-positivem NSCLC geprüft, die unter Crizotinib eine Tumorprogression erlitten hatten (»Journal of Clinical Oncology« 2017, DOI: 10.1200/JCO.2016.71.5904). Auch Patienten mit Hirnmetastasen wurden einbezogen, sofern sie neurologisch stabil waren und keine steigenden Corticosteroid-Dosen brauchten. Die Patienten erhielten entweder dauerhaft einmal täglich 90 mg oder sieben Tage lang 90 mg (Einleitungsphase), gefolgt von 180 mg einmal täglich. Die Nachuntersuchung dauerte median 22,9 Monate.
Die Patienten in der 90/180 mg-Gruppe schnitten durchweg besser ab. Die objektive Ansprechrate lag bei 56 Prozent (versus 46 Prozent) und die mediane Ansprechdauer bei 13,8 Monaten (versus 12). Das progressionsfreie Überleben (PFS) betrug 15,6 versus 9,2 Monate und das Gesamtüberleben 34,1 versus 29,5 Monate. Auch Patienten mit Hirnmetastasen sprachen auf die höhere Dosis besser an. Nebenwirkungen wie Nausea, Diarrhö, Kopfschmerzen und Husten waren meist leicht (Grade 1 bis 2).
In einer im November 2018 im »New England Journal of Medicine« veröffentlichten direkten Vergleichsstudie erhielten 275 ALK-positive NSCLC-Patienten, die noch keinen ALK-Hemmstoff bekommen hatten, entweder Brigatinib (90/180 mg einmal täglich) oder Crizotinib 250 mg zweimal täglich (DOI: 10.1056/NEJMoa1810171).
Zum Zeitpunkt der ersten geplanten Interimsanalyse lag das mediane Follow-Up bei elf Monaten in der Brigatinib-Gruppe und 9,3 Monaten in der Crizotinib-Gruppe. Signifikant mehr Patienten erfuhren unter Brigatinib keine Progression im Vergleich zu Crizotinib (67 versus 43 Prozent, geschätztes PFS nach zwölf Monaten). Auch die Ansprechrate war mit 71 versus 60 Prozent höher. Hirnmetastasen sprachen deutlich besser auf Brigatinib an.