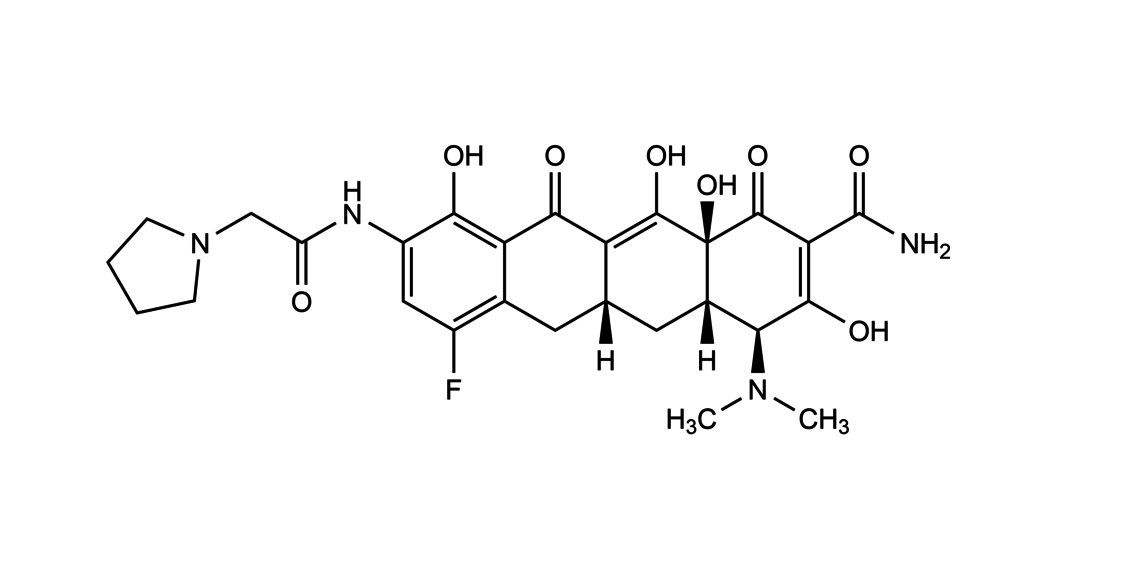
Eravacyclin wird als etwa 60-minütige intravenöse Infusion verabreicht. Die empfohlene Dosis beträgt 1 mg/kg Körpergewicht alle zwölf Stunden über einen Zeitraum von vier bis 14 Tagen.
Wie bei anderen Tetrazyklinen können schwere und gelegentlich tödliche Überempfindlichkeitsreaktionen auftreten. In solchen Fällen muss die Behandlung mit Eravacyclin sofort eingestellt und entsprechende Notfallmaßnahmen eingeleitet werden. Ebenfalls Wirkstoffklassen-typisch ist das Auftreten von Clostridioides-difficile-assoziierter Diarrhö. Unter diesen Umständen sollte erwogen werden, die Eravacyclin-Behandlung zu beenden und unterstützende Maßnahmen zusammen mit einer spezifischen Therapie von Clostridioides difficile einzuleiten. Arzneimittel, die die Peristaltik hemmen, sollten nicht gegeben werden. Antibiotika-spezifisch ist zudem das Auftreten einer Pankreatitis, die in einigen Fällen unter Xerava schwerwiegend verlief. Bei Verdacht auf diese Nebenwirkung sollte die Behandlung abgebrochen werden.
Eine längere Anwendung kann ein übermäßiges Wachstum nicht sensibler Mikroorganismen einschließlich Pilzen zur Folge haben. Tritt eine solche Superinfektion auf, muss die Therapie womöglich unterbrochen und eine alternative antimikrobielle Behandlung angewendet werden.