Molybdän-Cofaktor-Mangel (MoCD) ist eine äußerst seltene, erblich bedingte Stoffwechselstörung, die durch Mutationen in mehreren Genen verursacht wird. Patienten mit MoCD Typ A weisen Funktionsverlust-Mutationen im MOCS1-Gen auf, das für das Molybdän-Cofaktor-Biosyntheseprotein 1 (MOSC1) kodiert, und machen die Mehrheit der MoCD-Patienten aus.
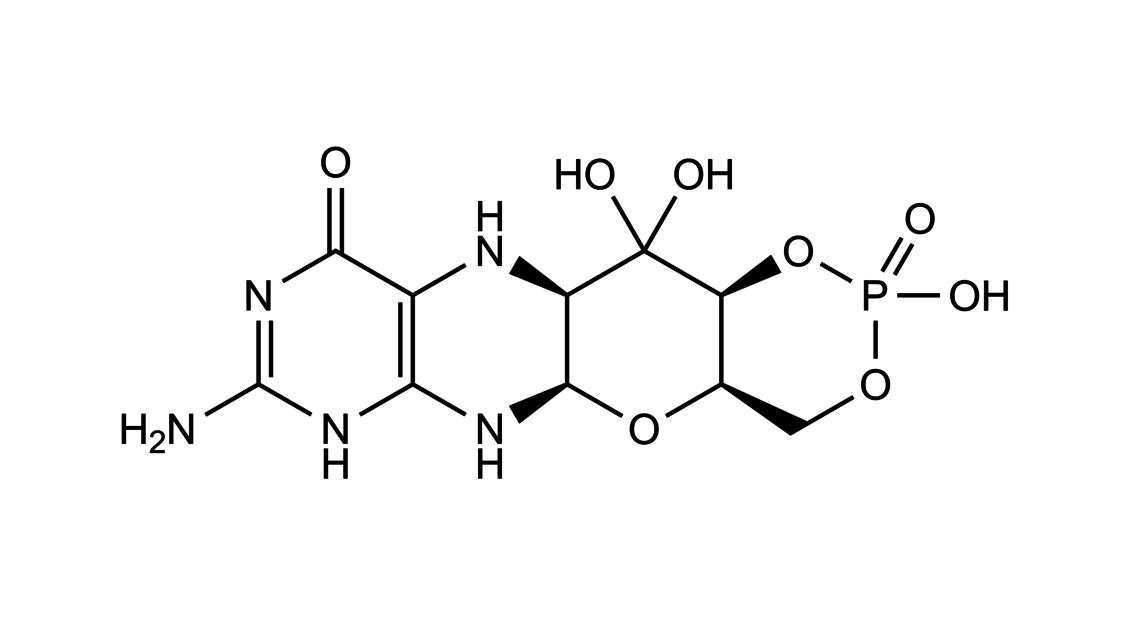
Fehlt funktionsfähiges MOCS1, kann der Körper auch das Zwischenprodukt zyklisches Pyranopterinmonophosphat (cPMP) nicht bilden. Dadurch wiederum ist der Molybdän-Cofaktor-(MoCo-)Stoffwechselweg gehemmt, was einen Mangel an funktionsfähiger Sulfitoxidase nach sich zieht und eine Anhäufung von toxischen Sulfiten im Gehirn bedingt.
Die Krankheit tritt in der Regel bei Neugeborenen auf und äußert sich durch hartnäckige Krampfanfälle, Wachstumsstörungen und andere Symptome, die einer raschen Neurodegeneration vorausgehen.