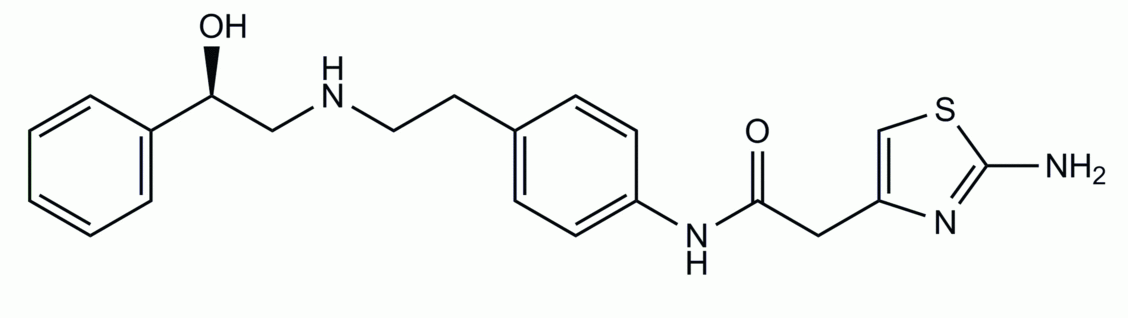
Mirabegron wird auf zahlreichen Wegen transportiert und metabolisiert. Es ist in vitro ein Substrat von CYP3A4, CYP2D6, Butyrylcholinesterase, UGT , PGP und OCT1, OCT2 und OCT3. Außerdem ist es ein mäßiger und zeitabhängiger Inhibitor von CYP2D6 und ein schwacher Inhibitor von CYP3A ist. Mirabegron hemmte in hohen Konzentrationen den über PGP vermittelten Wirkstoff-Transport.
Bei Patienten mit leichter bis mäßiger Einschränkung der Nierenfunktion oder leichter Einschränkung der Leberfunktion , die gleichzeitig starke CYP3A-Inhibitoren wie Itraconazol, Ketoconazol, Ritonavir oder Clarithromycin erhalten, beträgt die empfohlene Dosis 25 mg Mirabegron einmal täglich. Bei Patienten mit starker Einschränkung der Nierenfunktion oder mit mäßiger Einschränkung der Leberfunktion, die gleichzeitig starke CYP3A-Inhibitoren erhalten, wird Mirabegron nicht empfohlen.
Vorsicht ist geboten, wenn Mirabegron gemeinsam mit Arzneimitteln mit geringer therapeutischer Breite verabreicht wird, die in relevantem Maße durch CYP2D6 metabolisiert werden. Dazu gehören Thioridazin, Typ-1C- Antiarrhythmika (zum Beispiel Flecainid und Propafenon) und trizyklische Antidepressiva (zum Beispiel Imipramin unf Desipramin). Ebenso ist Vorsicht geboten bei gemeinsamer Anwendung von Mirabegron mit CYP2D6-Substraten, bei denen eine individuelle Dosiseinstellung erfolgt.
Mirabegron ist ein schwacher PGP-Inhibitor. Bei der Kombination mit sensitiven PGP-Substraten, beispielsweise Dabigatran, muss die potenzielle Hemmung von PGP durch Mirabegron berücksichtigt werden.
Ein Anstieg der Mirabegron-Exposition aufgrund von Wechselwirkungen kann mit einem Anstieg der Herzfrequenz verbunden sein.