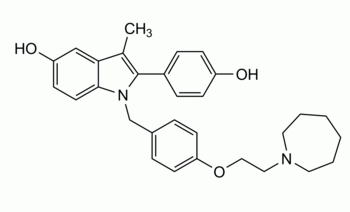
Kontraindiziert ist Bazedoxifen bei Frauen mit nicht abgeklärten Uterusblutungen und bei Anzeichen oder Symptomen eines Endometriumkarzinoms. Ferner ist der Wirkstoff nur bei Frauen nach der Menopause zugelassen, er darf nicht bei gebärfähigen Frauen zum Einsatz kommen. Gleiches gilt auch für Frauen mit bestehenden oder früheren venösen thromboembolischen Erkrankungen, einschließlich tiefe Venenthrombosen, Lungenembolie oder Retina-Venenthrombose. In der Fachinformation sind Risikofaktoren genannt, die in klinischen Studien mit einer venösen Thromboembolie assoziiert waren: fortgeschrittenes Alter, Adipositas, Immobilisierung, Operation, schweres Trauma und maligne Erkrankungen. Das erklärt, weshalb dazu geraten wird, das Arzneimittel vor und während längerer Immobilisierung, etwa nach einer Operation oder bei längerer Bettruhe, abzusetzen und die Behandlung erst nach vollständiger Wiederherstellung der Mobilität wieder aufzunehmen. Bei Patientinnen mit schweren Nierenproblemen sollte der Arzt Bazedoxifen nur mit Vorsicht einsetzen, bei Leberproblemen gar nicht.
Bei Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Inhaltsstoffe ist das Arzneimittel kontraindiziert.