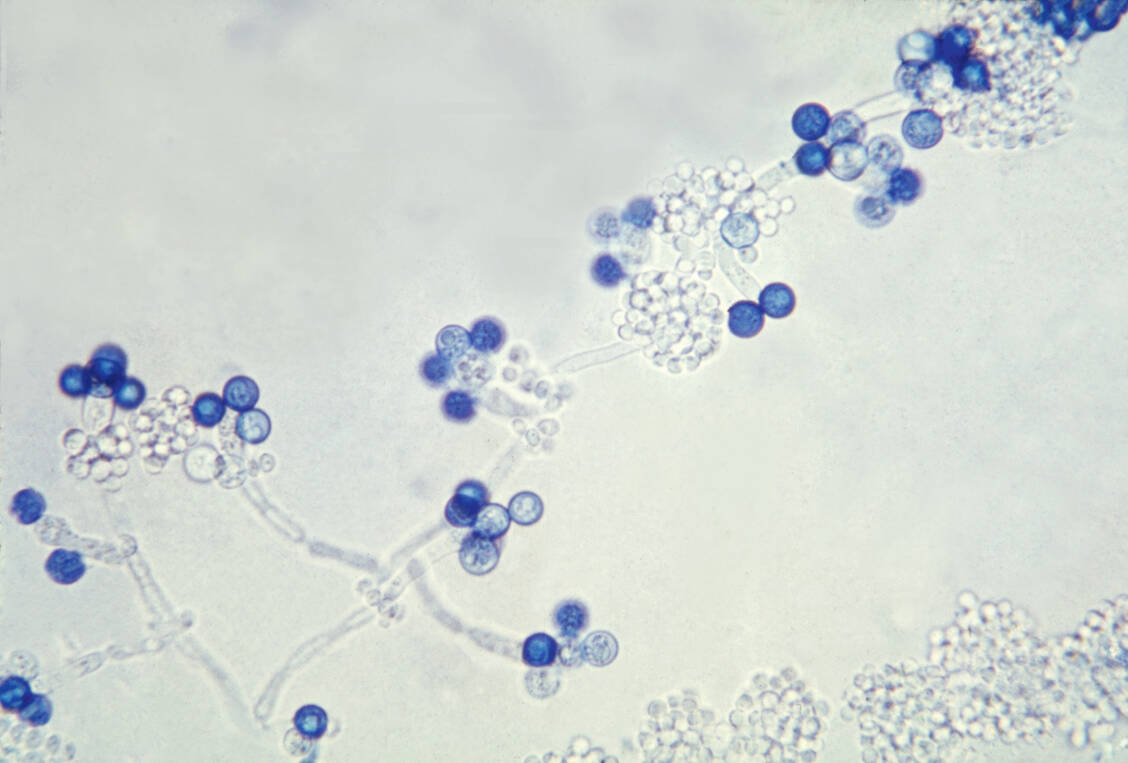
Die Autoren nutzten für ihre Analyse eine nationale niederländische und internationale Nebenwirkungs-Datenbanken der Weltgesundheitsorganisation (WHO) und der Europäischen Arzneimittelagentur (EMA) sowie Daten einer an ihrer eigenen Universität betreuten Kohorte von mit Biologika behandelten Psoriasis-Patienten. Dabei zeigte sich, dass in der WHO-Datenbank zu IL-17-Hemmern zehnmal so häufig Candidosen als Nebenwirkung gemeldet wurden wie zu TNF-α-Inhibitoren (10,2-mal so viele Berichte registriert), insbesondere für Candidosen der Haut (12,3-mal so viele Einträge), des Mund- und Rachenraums (Faktor 19,2) und der Speiseröhre (Faktor 21,2). Hieraus ergab sich ein je nach Art der Candidose vier- bis zehnfach erhöhtes Risiko gegenüber TNF-α-Blockern, welches die EMA-Daten (16- bis 33-fach erhöhtes Risiko), das nationale Register (zwei- bis 42-facher Risikoanstieg) und die Kohortenstudie (drei- bis 25-fache Erhöhung) bestätigten. Wurde bei einem Patienten eine Anti-IL-17-Therapie begonnen, steigerte das sein Risiko für eine behandlungsbedürftige Candidose um das Zwei- bis 16-Fache.