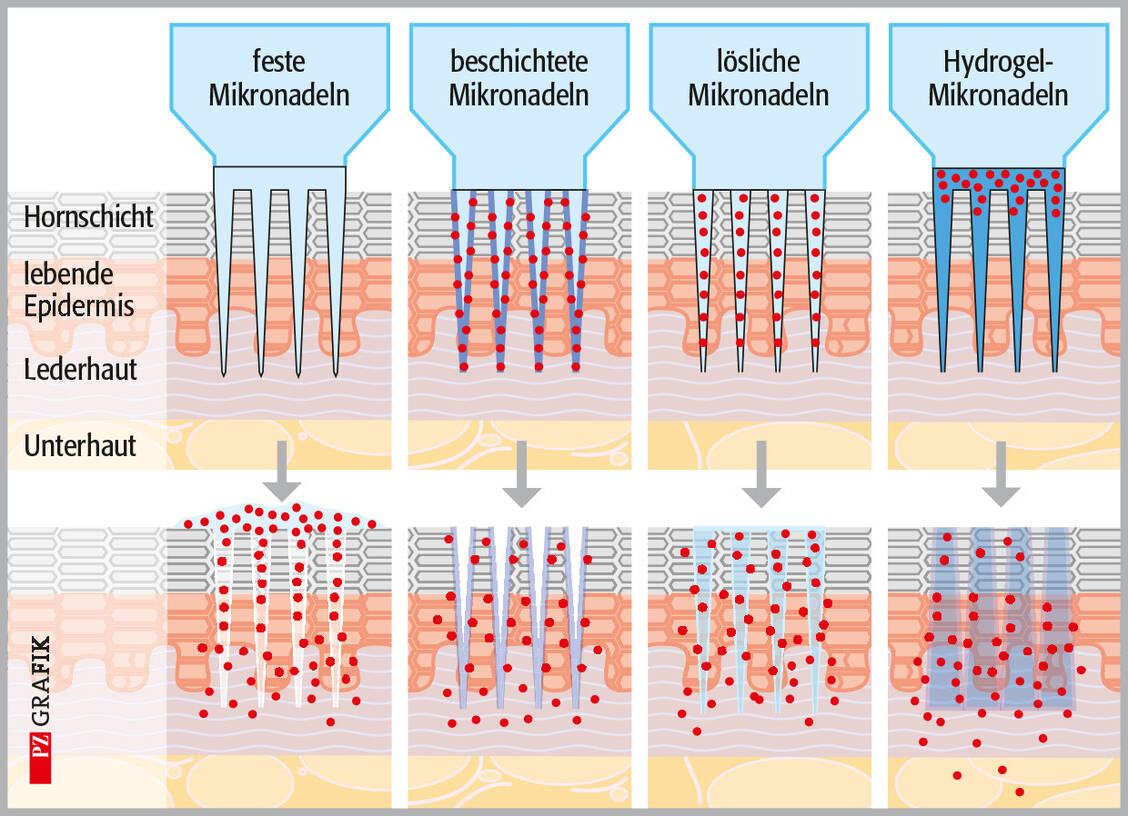
In Deutschland sind einige medizinische Mikronadelprodukte wie SkinPen® Precision, Dermida NeedlingPen oder XCellaris Pro Twist für die Behandlung von Narben und Falten sowie zur Kollagenstimulation als Medizinprodukte zertifiziert. Sie dürfen von Ärzten oder geschultem medizinischen Personal angewendet werden. Neben dem rein physikalischen Effekt des Microneedlings sehen die jeweiligen Produktbeschreibungen auch die Applikation kosmetischer Wirkstoffe, meist in Form von Konzentraten, vor. Ebenfalls kommerziell erhältlich und für den Gebrauch zu Hause gedacht sind Mikronadelpflaster mit Hyaluronsäure.
Kommerzielle Anbieter vertreiben Mikronadel-Array-Pflaster als Plattformtechnologie für die Wirkstoffapplikation, beispielsweise die AccuTip-MAP-Plattform von LTS. Das Potenzial solcher Technologien wurde bereits in präklinischen und klinischen Phase-I-Studien gezeigt.