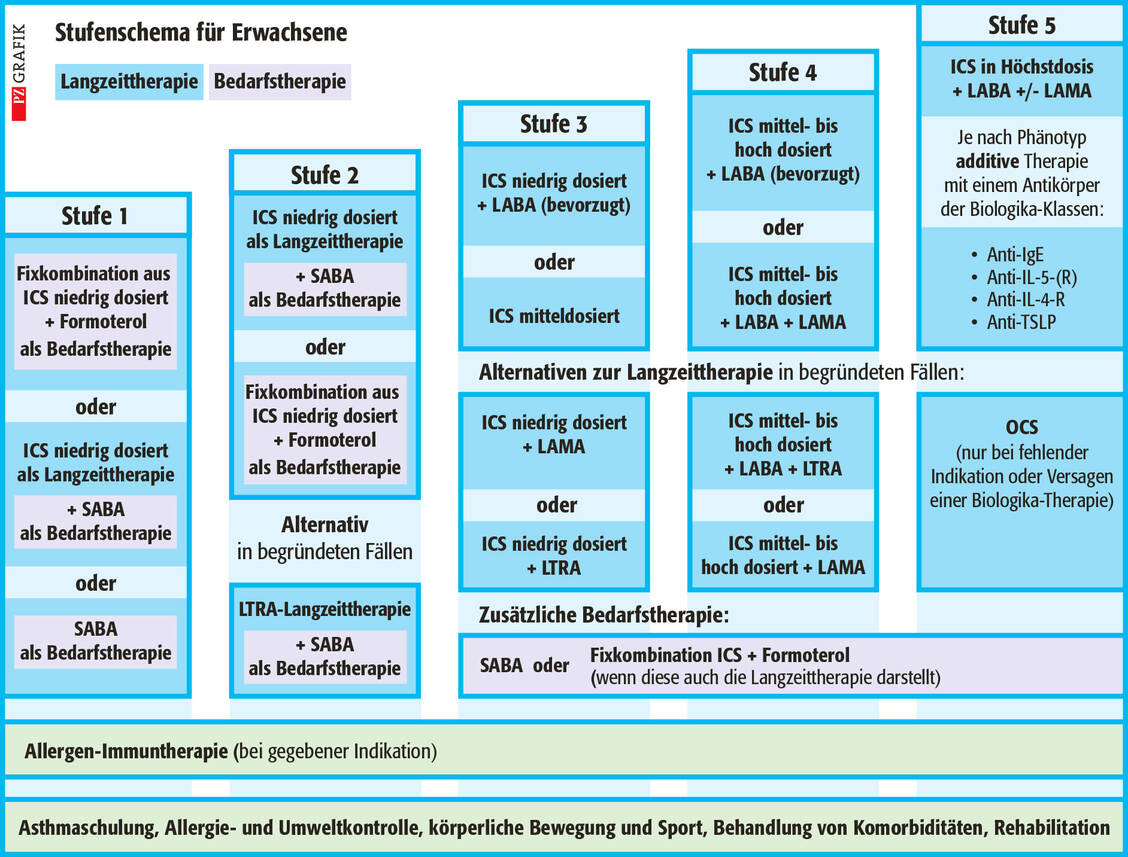
Beta-2-Sympathomimetika sind und bleiben die favorisierten Bronchodilatatoren in der Asthmatherapie: kurz wirksame (SABA) oder lang wirksame (LABA). Neu ist die höhere Bewertung einer Fixkombination aus ICS (niedrig dosiert) plus LABA (Formoterol) bereits ab Stufe1 als Bedarfstherapie und ab Stufe 2 als Dauertherapie, wobei für den Bedarf zusätzlich ICS/SABA-Kombinationen, zum Beispiel mit Salbutamol, zum Einsatz kommen. In den seltenen Fällen einer Unverträglichkeit von LABA-Kombinationen können ab Stufe 3 in Einzelfällen auch lang wirksame Muskarin-Antagonisten (LAMA, insbesondere Tiotropiumbromid) zum Einsatz kommen. Durch die neue, langfristig angelegte Kombinationstherapie ist auch die klassische Einteilung der Therapeutika in »Controller« (nur Entzündungshemmung) und »Reliever« (akute Symptombehandlung) überholt. Diese Vorgaben decken sich mit den Empfehlungen, die bereits in der 4. Auflage der Nationalen Versorgungsleitlinie Asthma 2020 getroffen wurden (9).