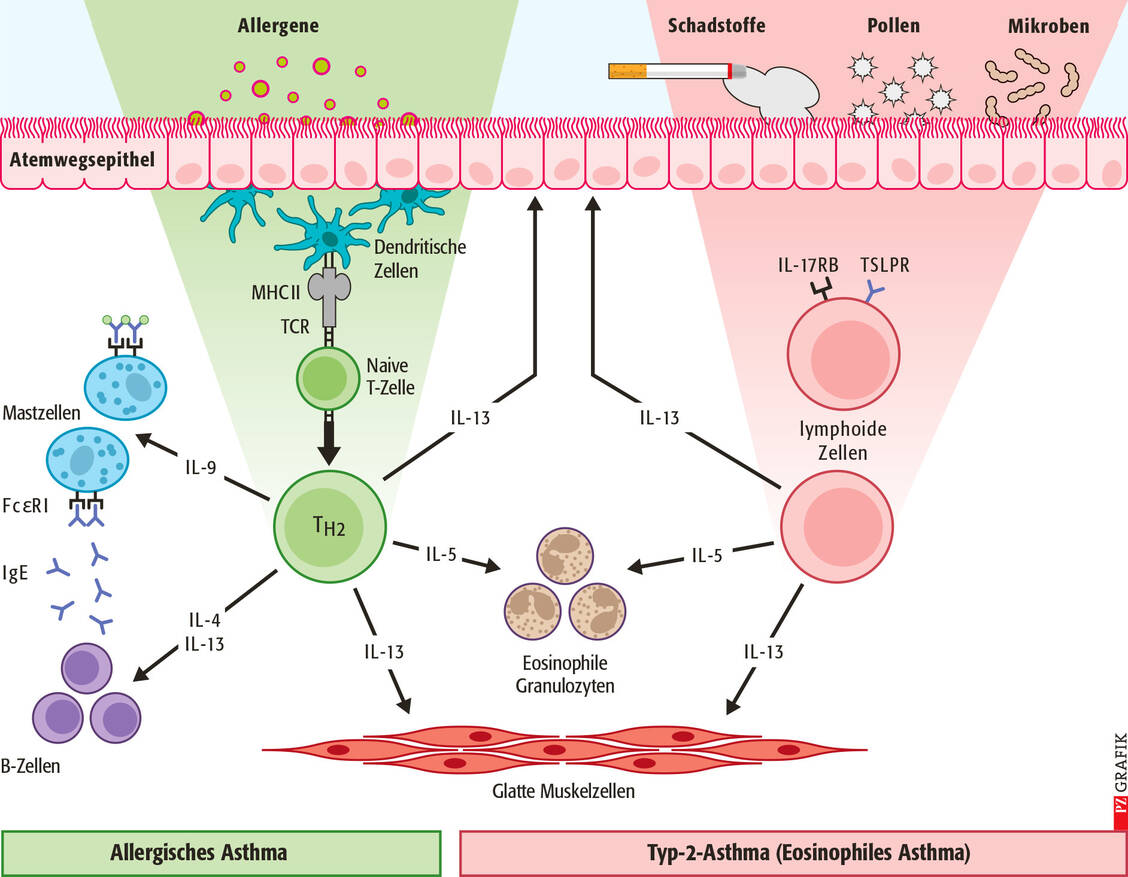
Diese Phänotypisierung verbessert eine zielgerichtete Therapie und hat insbesondere für die Behandlung schwerer Verlaufsformen große Relevanz. Ein allergisches Asthma ist gekennzeichnet durch erhöhte Level an Immunglobulin E (IgE) oder den Interleukinen IL-4 und -13. Doch auch nicht allergische Trigger können die Entzündungskaskaden forcieren. Da bestimmte Zytokine, insbesondere IL-5 und IL-13, nicht nur von Allergen-spezifischen TH2-Zellen des adaptiven Immunsystems, sondern auch von Allergen-unspezifischen lymphoiden Zellen des angeborenen Immunsystems freigesetzt werden, fasst man diese beiden Phänotypen der asthmatischen Entzündung neuerdings unter dem Oberbegriff »Typ-2-Asthma« zusammen (Abbildung 1, rechts). Die Aktivierung von Eosinophilen ist ein wichtiger Entzündungstrigger (4).