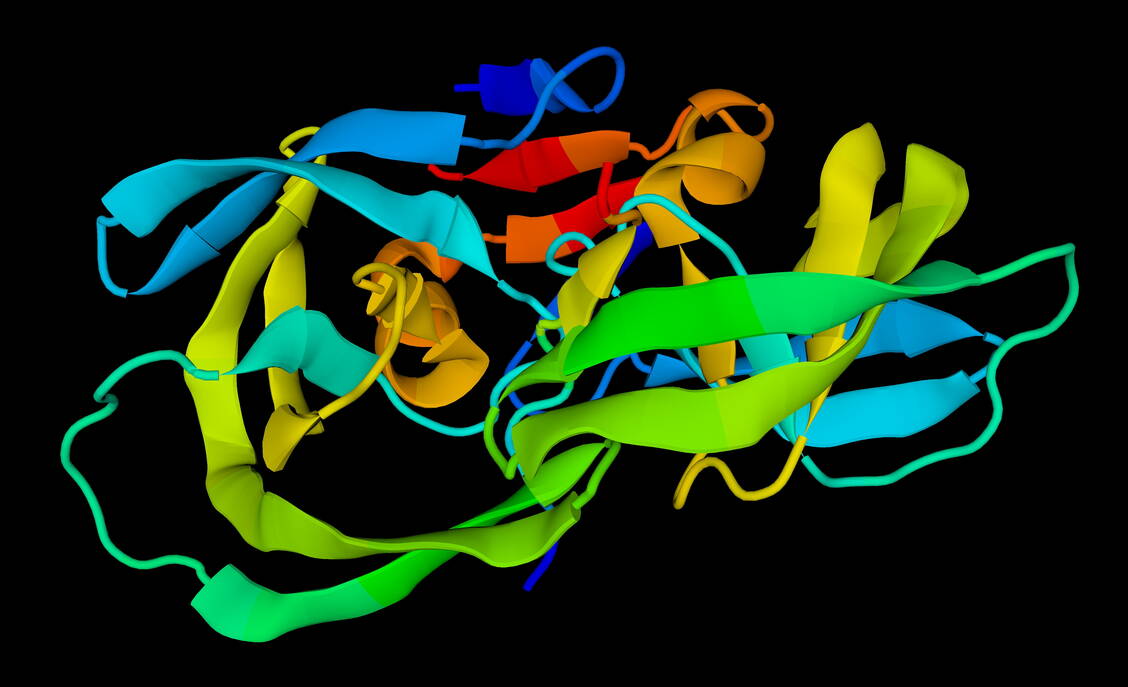
Die HIV-Protease war 1989 erstmals strukturell durch Röntgenkristallografie charakterisiert worden. Die Beobachtung, dass der Aspartatprotease-Hemmer Pepstatin ebenfalls die HIV-Protease zu hemmen vermochte, setzte eine intensive Suche nach geeigneten HIV-Protease-Inhibitoren in Gang, an der sich fast alle wichtigen Pharmakonzerne beteiligten. Die Entwicklung der Vertreter dieser Wirkstoffklasse, die bis auf Tipranavir alle den Peptidmimetika zuzuordnen sind, war auch deshalb bemerkenswert, da hier in großem Stil das damals relativ neue Konzept eines weitgehend auf Röntgenkristallstrukturanalysen der Protease basierten rationalen Drug Designs eingesetzt wurde. So gelang den Wissenschaftlern bei Roche der Nachweis, dass sich allein durch Ersatz der zentralen Amidbindung der peptidischen Inhibitor-Kandidaten durch eine Hydroxyethylamino-Gruppe, die den beim Spaltmechanismus auftretenden tetraedrischen Übergangszustand nachahmt, hochaffine Hemmstoffe erhalten ließen.