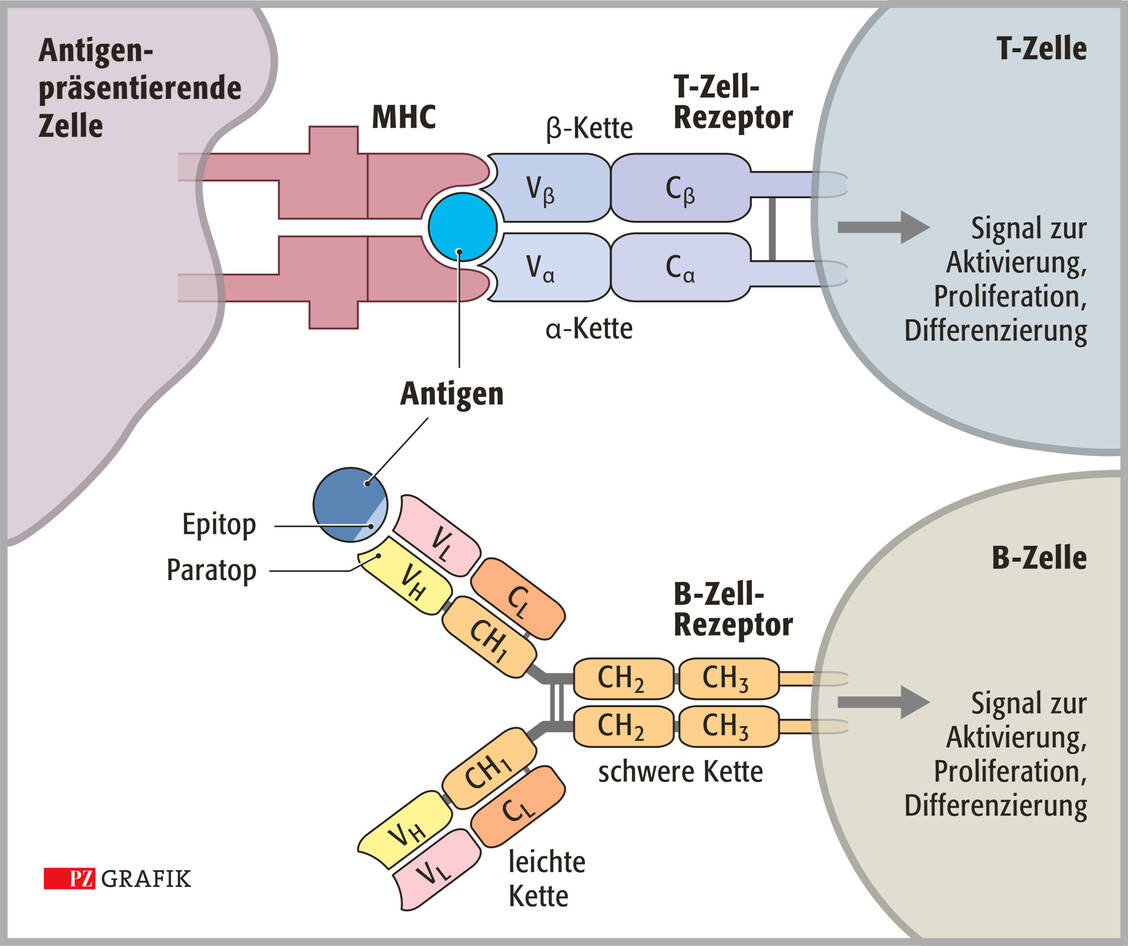
Betrachtet man diese Zahlen an unterschiedlichen Rezeptoren, passt das nicht zu der Erkenntnis, dass der Mensch nur zwischen 20.000 und 25.000 Gene hat. Interessanterweise codiert nur eine Handvoll Gene für die Erkennungsrezeptoren, dennoch sind ihre Antigenerkennungsdomänen enorm vielfältig. Für diese Diskrepanz ist die sogenannte somatische Rekombination verantwortlich: Ähnlich einem Baukastensystem werden einzelne Genabschnitte nach dem Zufallsprinzip so umgelagert, dass eine Vielzahl an T- und B-Lymphozyten entsteht, die sich nur in den variablen Bereichen dieser Rezeptoren unterscheiden. Zusätzlich führen Ungenauigkeiten bei Reparaturmechanismen während dieser Umlagerung zu weiteren Variationen bei den Antigenrezeptoren.