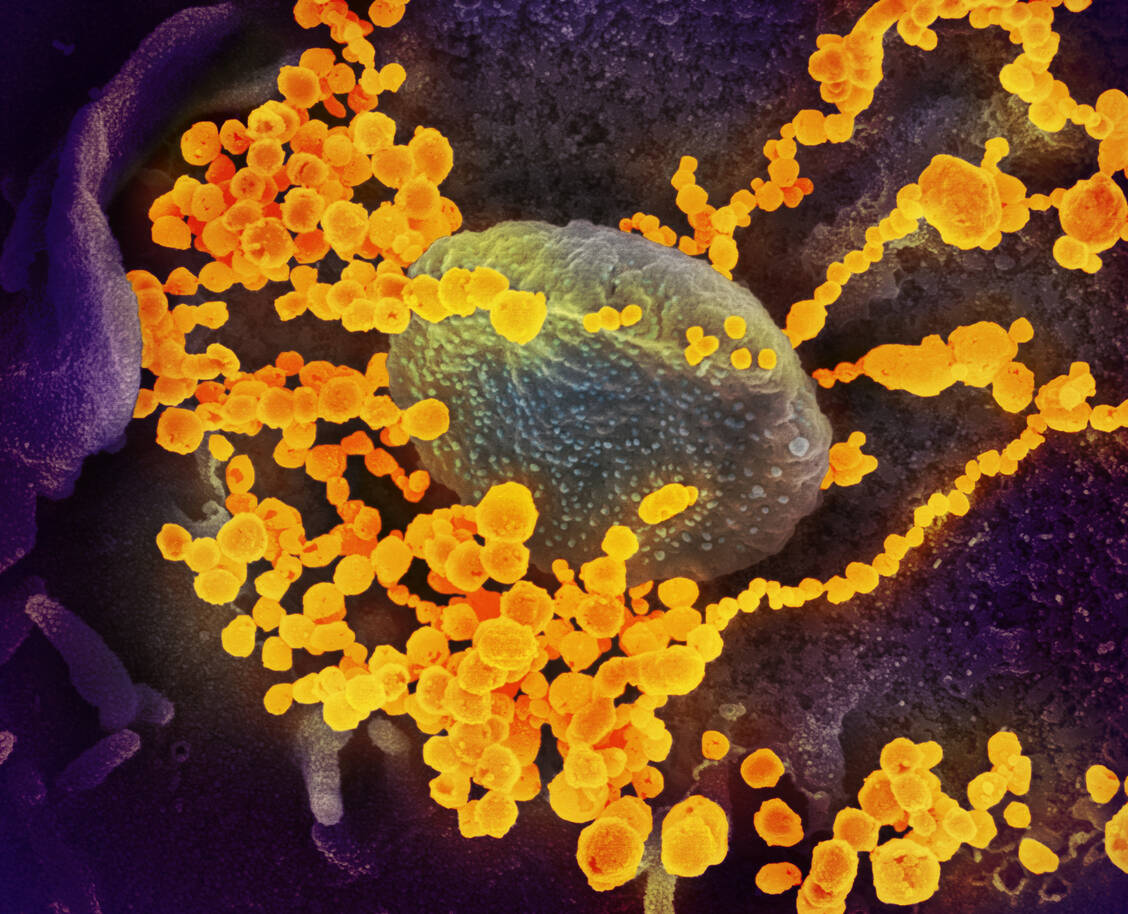
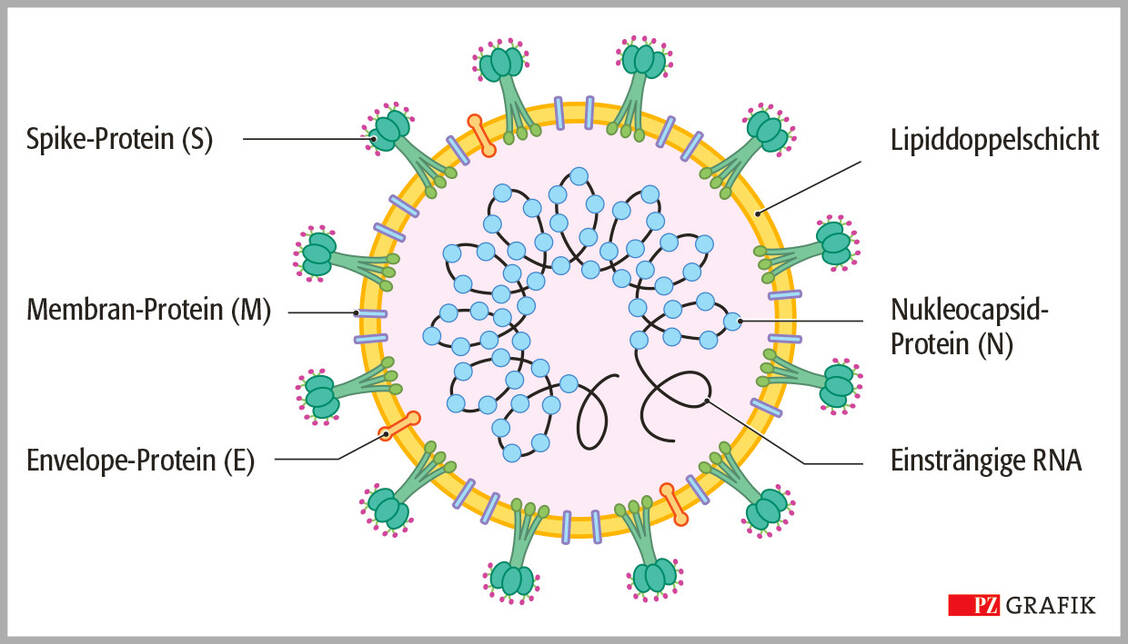
SARS-CoV-2 wird aus vier Strukturproteinsorten aufgebaut: S (Spike), M (Membrane), E (Envelope) und N (Nucleocapsid). Die N-Proteine umschließen den inneren Bereich und beinhalten das RNA-Genom (siehe Abbildung). S, E und M bauen gemeinsam die äußere Hülle auf. Alle Proteine an der Oberfläche sind denkbare Antigene und können für die Entwicklung potenzieller Impfstoffe von großer Bedeutung sein. Am prominentesten ist sicher das S-Protein, das den Oberflächenkontakt des Virus zur Wirtszelle über den ACE2-Rezeptor herstellt.
Das S-Protein ist ein Homotrimer aus ineinander verflochtenen Monomeren (»Cell«, DOI: 10.1016/j.cell.2020.02.058). Die Strukturproteine E und M können ebenso für die Entwicklung potenzieller Impfstoffe von Bedeutung sein, da sie wichtige Rollen beim Eindringen des Virus in die Wirtszelle oder beim Zusammenbau des Virus spielen. E ist ein kationenselektiver Ionenkanal und wichtig beim Zusammenbau des Virus. Wenn es fehlt, entstehen attenuierte Viren. M ist der Hauptbestandteil der stabilisierenden Außenmembran und ähnelt häufig den Membranproteinen der Wirtszellen.