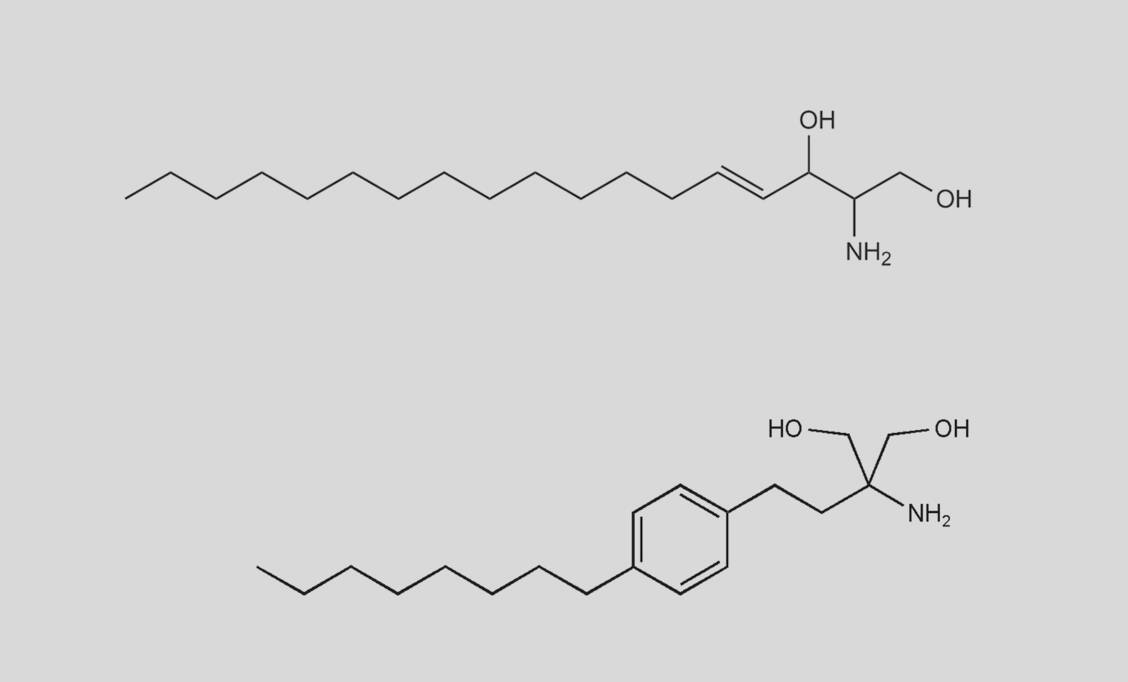
Nach oraler Gabe wird Fingolimod zu 93 Prozent aufgenommen und ähnlich wie endogenes Sphingosin durch eine Sphingosinkinase phosphoryliert und damit aktiviert. Das resultierende Fingolimod-Phosphat wirkt dann zunächst genauso wie Sphingosin-1-Phosphat als Agonist an S1P-Rezeptoren, bewirkt dann aber durch seine langdauernde Rezeptorbindung eine Downregulation und Internalisierung des Rezeptors mit anschließendem intrazellulärem Rezeptorabbau. Über diesen Mechanismus wird Fingolimod-Phosphat zum funktionellen Antagonisten, der die physiologischen Funktionen von S1P abschaltet. Damit fehlt den antigenaktivierten, autoreaktiven Lymphozyten das Austrittssignal aus den Lymphknoten und es resultiert eine periphere Lymphopenie, die auch die Rezirkulation der Lymphozyten in das Gehirn unterbricht. So werden bei der MS akute Schübe durch zentrale Entzündungsherde verhindert.