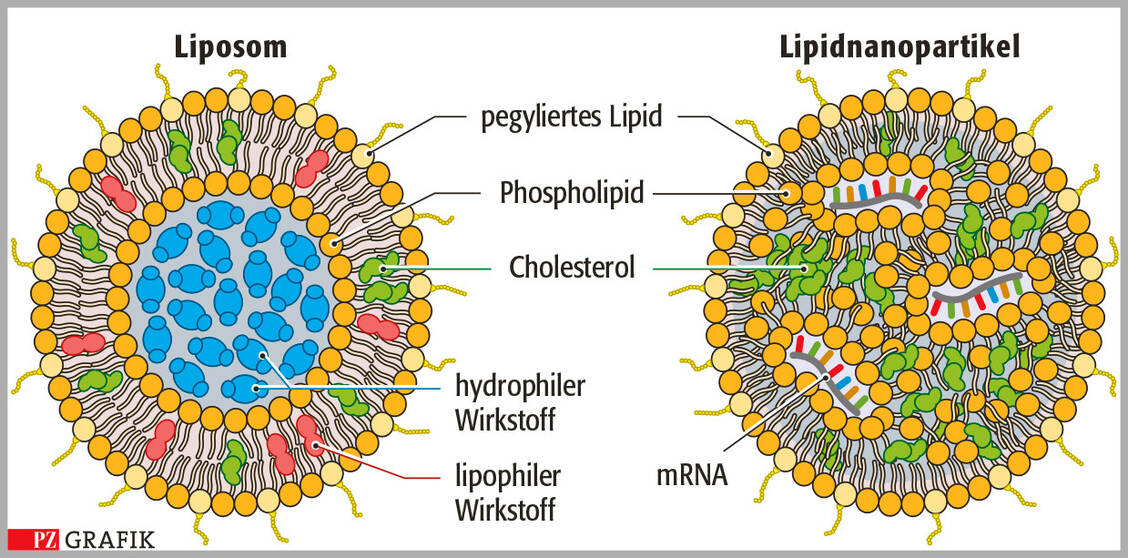
Als Wirkstoff enthält der Impfstoff ebenfalls eine Einzelstrang-mRNA, die für das virale Spike-(S-)Glykoprotein von SARS-CoV-2 codiert (Abbildung 3).
Jedes Mehrdosenbehältnis beinhaltet gemäß EMA Assessment Report zehn Impfdosen zu je 0,5 mL (10). Die Vials sind mit einem Gesamtfüllvolumen von 6,3 mL um 1,3 mL überfüllt und würden die theoretische Entnahme von zwölf Dosen ermöglichen. Allerdings ist eine Entnahme von mehr als zehn Impfdosen gegenwärtig nicht vorgesehen. Eine Impfdosis enthält 100 µg mRNA eingebettet in »SM-102 Lipid-Nanopartikel«. Hierbei handelt es sich um LNP-Strukturen, die nach dem kationischen Lipid SM-102 benannt sind. Der Impfstoff ist »ready to use« und erfordert keine weiteren Verdünnungs- oder Rekonstitutionsschritte. Für eine Immunisierung werden zwei Injektionen im Abstand von 28 Tagen empfohlen.
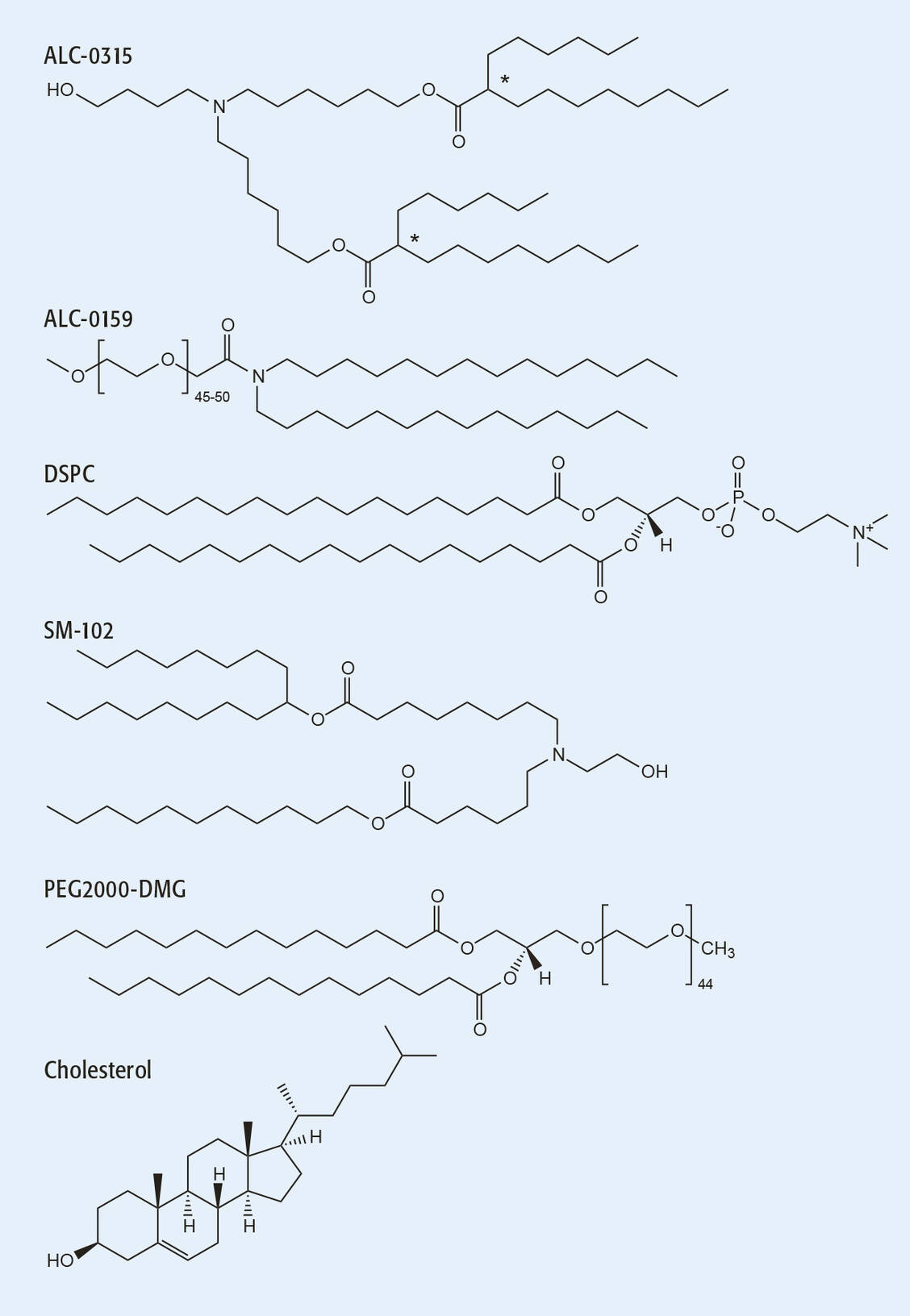
Die Lipidzusammensetzung der LNP ähnelt in der Auswahl dem Impfstoff Comirnaty®. Auch bei dem Impfstoff von Moderna werden drei Lipide für den Aufbau des Partikelsystems verwendet (Tabelle 1). Das amphotere und damit nach außen ungeladene Lipid DSPC dient zusammen mit Cholesterol als Strukturkomponente dem Partikelaufbau. Bei SM-102 handelt es sich wie bei ALC-0315 um ein tertiäres Amin, das bei physiologischem pH-Wert ungeladen vorliegt und bei der Herstellung der mRNA-Bindung über elektrostatische Wechselwirkungen dient. Als PEG-Derivat wird in der Vakzine PEG2000-DMG verwendet, das der sterischen Stabilisierung der LNP-Struktur dient und die Immunerkennung der Nanopartikel minimiert.
Auch bei der Moderna-Vakzine stellen die beiden funktionellen Lipide SM-102 und PEG2000-DMG neuartige Hilfsstoffe dar, die bisher noch nicht in zugelassenen Fertigarzneimitteln zu finden waren. Allerdings wurde in dem 2018 zugelassenen Fertigarzneimittel Onpattro® mit PEG2000-C-DMG ein strukturell sehr ähnliches Lipid zu LNP verarbeitet, für das ein Risiko der Antikörperbildung gegen PEG beschrieben ist (11).
Die Lipidnanopartikel werden in mehreren Arbeitsschritten hergestellt (10, 12) (Abbildung 3). Zunächst wird eine alkoholische Lipidstammlösung hergestellt und diese in einem Mikrofluidik-System, zum Beispiel: NanoAssemblr™ (13), über Pumpensysteme mit einer wässrigen mRNA-Lösung gemischt. Über das Prinzip der Nanopräzipitation entsteht eine LNP-Dispersion, die anschließend mittels Tangentialflussfiltration (TFF) gereinigt wird, um das organische Lösungsmittel abzutrennen. Nach Zusatz des Kryoprotektors Saccharose und einer weiteren Filtration erfolgt die Abfüllung in Vials und das Einfrieren der Zubereitung. Für den fertigen Impfstoff wird aktuell eine Lagerzeit von sieben Monaten bei –20 °C, einschließlich einer 30-tägigen Lagerung bei 2 bis 8 °C, angegeben.
Pharmakokinetische Untersuchungen erfolgten im Tierversuch an der Ratte. Neben einer Anreicherung der mRNA am Injektionsort konnte der Wirkstoff in allen untersuchten Geweben außer der Niere wiedergefunden werden. Eine Umverteilung in die Leber ist für Lipid-basierte Nanopartikel typisch und wurde auch für die Moderna-Vakzine beobachtet. Besonders bemerkenswert erscheint der Nachweis geringer mRNA-Konzentrationen im Gehirn, ein Hinweis auf einen Transport der Nanopartikel über die Blut-Hirn-Schranke.