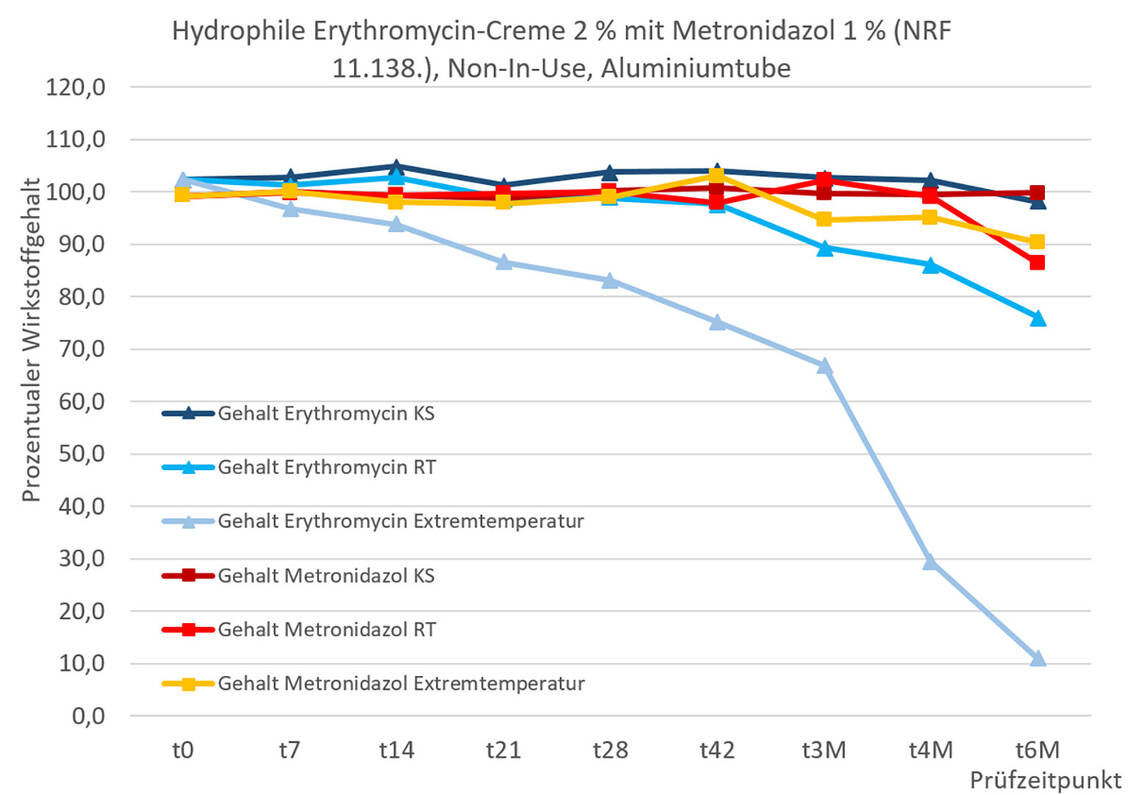
Die Grundlage ist eine verdünnte Basiscreme DAC, die zuvor mit 0,5-prozentiger Citronensäure-Lösung versetzt wird, um in der fertigen Zubereitung einen pH von etwa 8 einzustellen. Somit bietet die Creme ein akzeptables Milieu sowohl für Erythromycin, dessen rezeptierbarer pH-Bereich für Suspensions-Zubereitungen nach den DAC/NRF-Tabellen für die Rezeptur zwischen 7 und 10 liegt, als auch für Metronidazol, das generell zwischen pH 3 und 8 verarbeitet werden darf. Vor der anteiligen Zugabe der Grundlage werden die beiden mikronisierten Wirkstoffe in der Fantaschale mit Glycerol angerieben. Während Metronidazol in der Creme größtenteils gelöst vorliegt, ist der überwiegende Teil von Erythromycin suspendiert. Die Lagerung der fertigen Rezeptur soll im Kühlschrank bei ≤ 8 °C erfolgen. Die Aufbrauchsfrist wird mit vier Wochen angegeben.