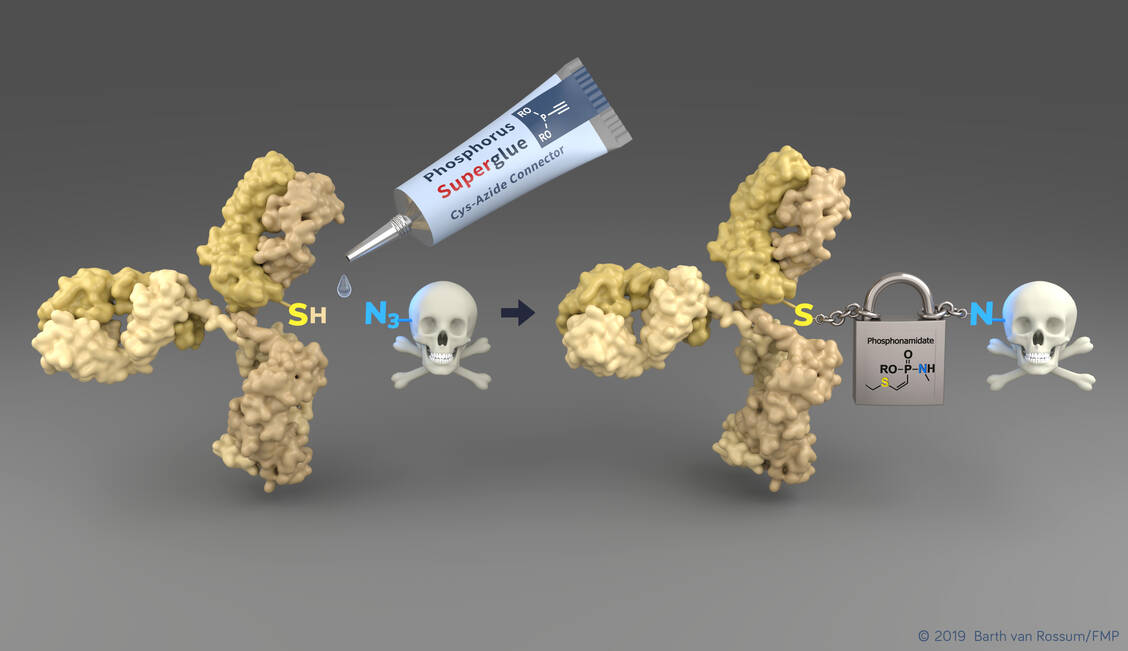
Die Forscher nutzen eine besondere Eigenschaft ungesättigter Phosphor-(V)-Verbindungen aus. Die sogenannten Phosphonamidate verbinden eine gewünschte Modifikation, zum Beispiel einen zytotoxischen Wirkstoff, ausschließlich mit der Aminosäure Cystein in einem Protein. Da es sich bei Cystein um eine sehr seltene natürliche Aminosäure handelt, kann die Anzahl an Modifikationen pro Protein sehr gut kontrolliert werden, was für die Herstellung von Wirkstoff-Konjugaten unerlässlich ist. Zudem lassen sich Phosphonamidate sehr einfach auch in komplexe chemische Verbindungen einbauen. »Die größte Errungenschaft der neuen Methode ist allerdings, dass die so entstandene Bindung auch während der Zirkulation im Blut stabil ist«, so Kasper. Die heute verfügbaren Antikörper-Wirkstoff-Konjugate könnten dies nicht leisten.