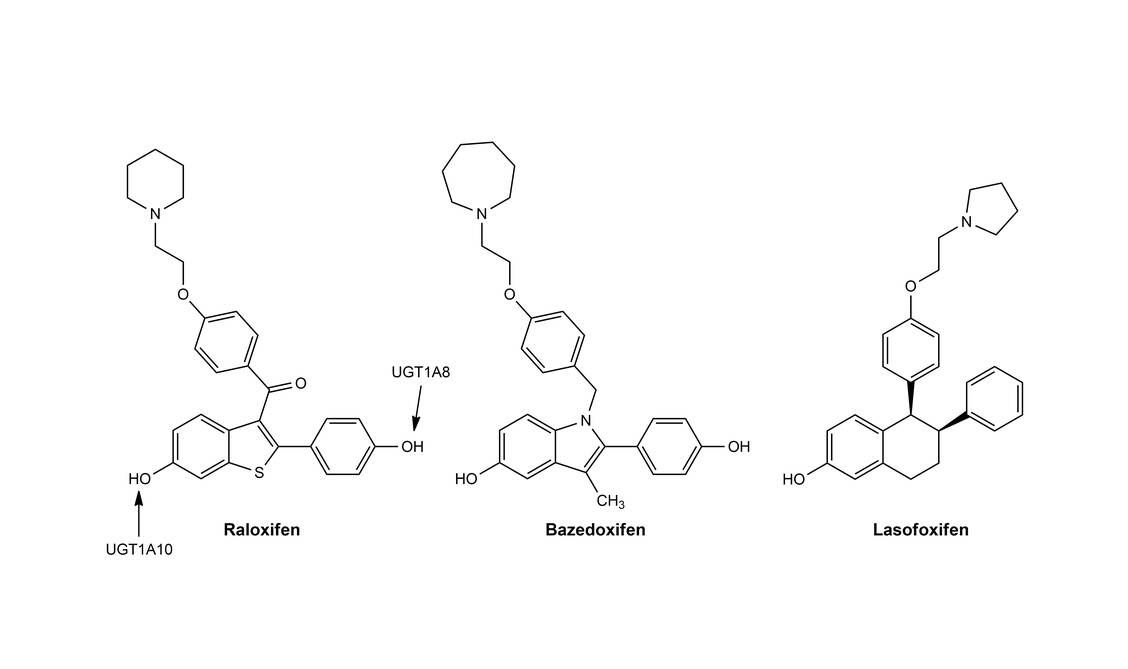
Tamoxifen kann man als »First-in-class«-SERM betrachten, das zur Behandlung von Hormon-abhängigem Brustkrebs eingesetzt wird. Schon kurz nach der Markteinführung von Nolvadex® fiel auf, dass nicht alle Patientinnen gleichermaßen von der Therapie profitierten. Dies lässt sich mit dem Metabolismus erklären.
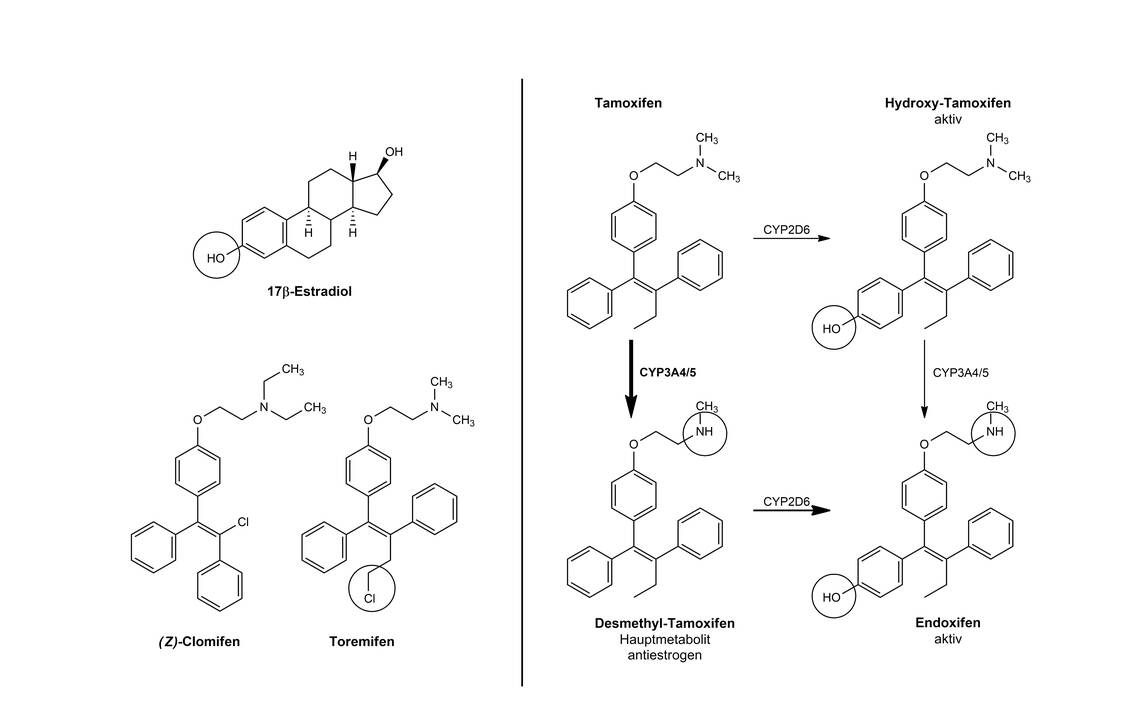
Tamoxifen fehlt die Hydroxylgruppe, die der Phenolstruktur (Ring A) des Estradiols entspricht, und bindet deshalb deutlich schwächer an den ER (1000-fach schwächer als sein Metabolit Hydroxytamoxifen). Tamoxifen ist also ein Prodrug und muss durch Cytochrom-P450-2D6 aktiviert, das heißt hydroxyliert werden. CYP2D6 ist für seinen Polymorphismus bekannt. Eine Reihe von Menschen sind sogenannte »poor metabolizer«, das heißt: Diese Hydroxylierung zu Hydroxytamoxifen und letztlich Endoxifen findet bei ihnen kaum oder nicht statt (Abbildung 4). Daher ist es wichtig, dass vor einer Tamoxifen-Therapie eine Genotypisierung der Patientin erfolgt, um den Therapieerfolg zu ermöglichen (5).