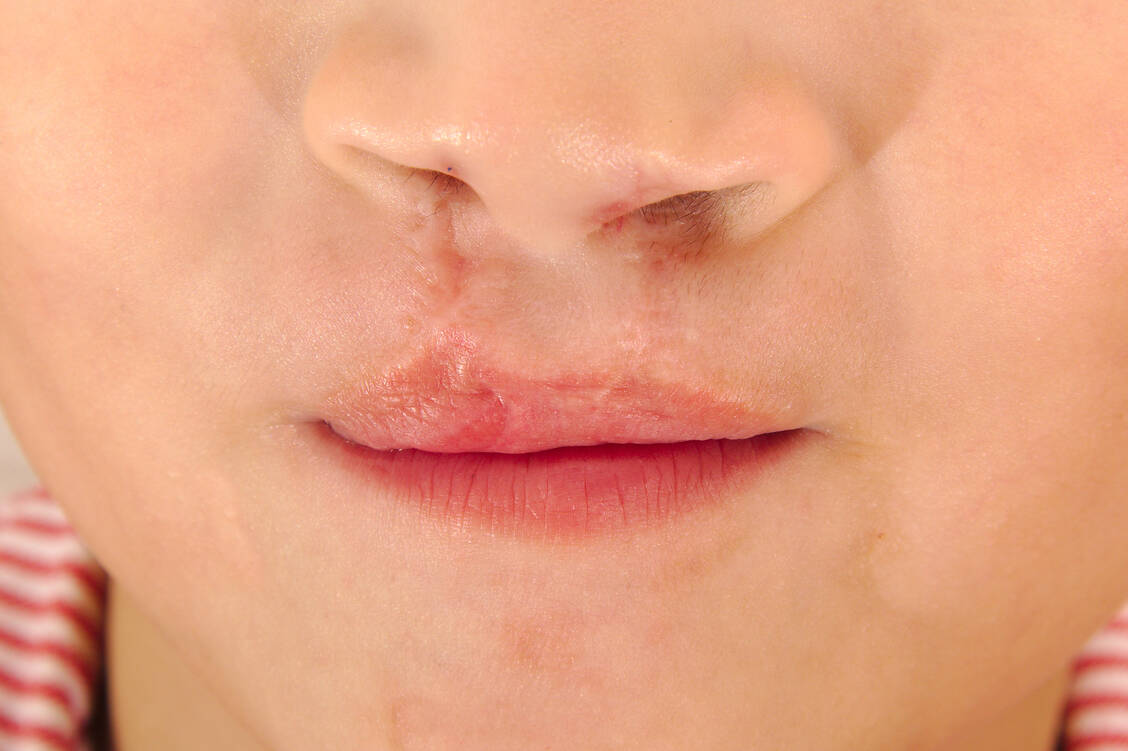
Ondansetron ist ein 5- HT3-Rezeptorantagonist, der gegen Übelkeit und Erbrechen hilft. Er ist aber nicht für die Behandlung von Schwangerschaftsübelkeit oder Hyperemesis gravidarum zugelassen – zu Recht, wie neue Daten aus epidemiologischen Studien zeigen. »In einer Kohortenstudie mit 1,8 Millionen Schwangeren war die Anwendung von Ondansetron im ersten Trimenon mit einem erhöhten Risiko für Lippen-, Kiefer-, Gaumenspalten verbunden«, heißt es in einem aktuellen Rote-Hand-Brief. Demnach traten drei zusätzliche Fälle pro 10.000 behandelten Frauen auf (adjustiertes relatives Risiko 1,24 (95%-KI 1,03-1,48)). Möglicherweise kann es auch zu Herzfehlbildungen kommen, hier seien die Daten jedoch widersprüchlich.