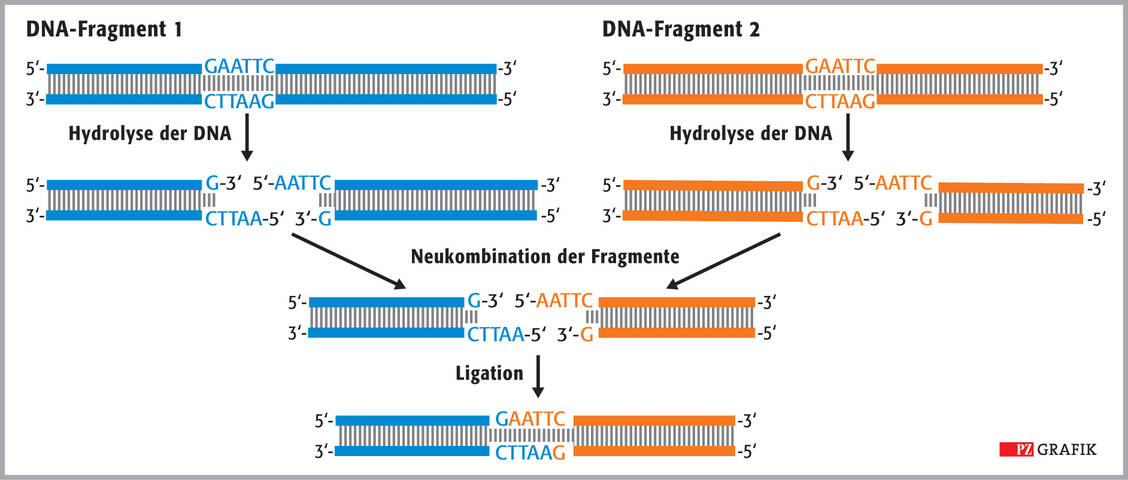
Der nächste Schritt war die Entdeckung, dass sich Bakterien mittels sogenannter Restriktionsenzyme gegen die durch Phagen eingebrachte DNA verteidigen. Zunächst identifizierten Werner Arber und Matthew Meselson in den 1960er-Jahren die Typ-I-Restriktionsendonukleasen, die eine DNA an einer bestimmten Stelle erkennen, aber dann zufällig in einiger Entfernung davon einen Schnitt in den Doppelstrang setzen. Als wesentlich hilfreicher für die Molekularbiologen erwiesen sich Typ-II-Restriktionsenzyme. Diese Art Endonuklease erkennt und schneidet eine sehr spezifische, vier bis acht Nukleotide lange Basenabfolge innerhalb der DNA, die eine doppelte Symmetrie aufweist. Schneidet man verschiedene DNA-Moleküle mit demselben Enzym, entstehen jeweils die gleichen Enden, die anschließend wie passende Steckverbindungen neu verknüpft werden können (Abbildung 1). Das dazu benötigte Enzym, eine sogenannte DNA-Ligase, hatten Bernard Weiss und Charles C. Richardson bereits 1967 beschrieben.
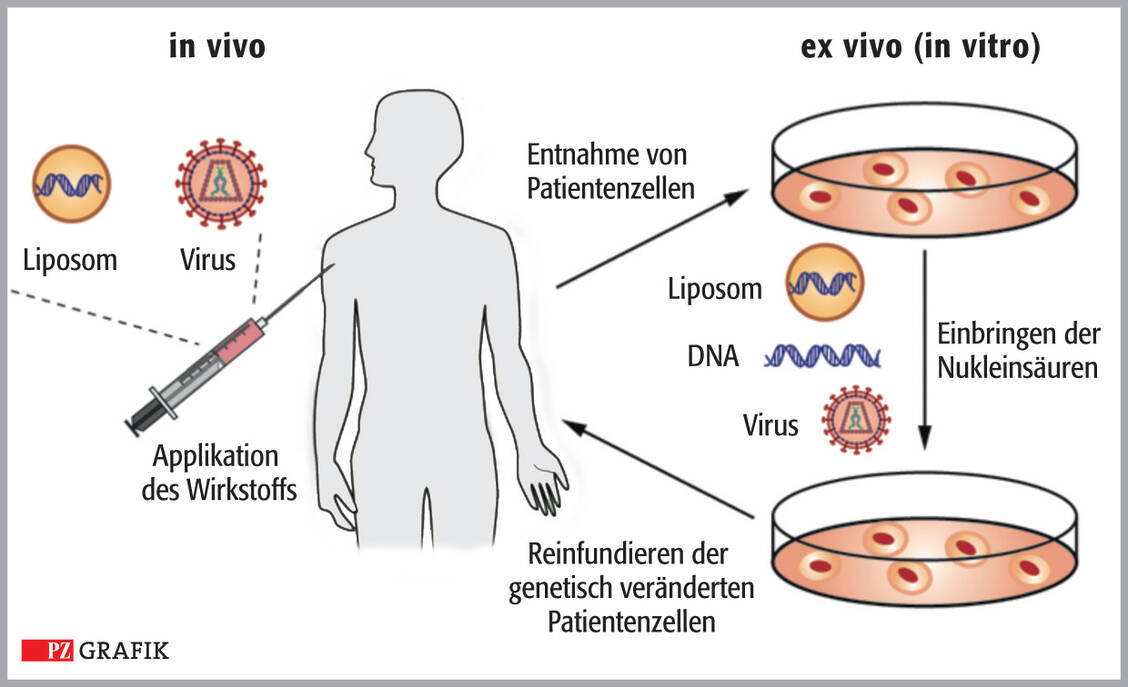
Jetzt waren alle Voraussetzungen geschaffen, DNA neu zu kombinieren und damit gentechnisch veränderte Organismen (GVO) herzustellen (Abbildung 2) – ein Experiment, das Herbert Boyer und Stanley Cohen zusammen mit Annie Chang und Robert Helling im Jahr 1973 publizierten, nur 20 Jahre nach Aufklärung der DNA-Struktur. Das war damals mit den mageren technischen Möglichkeiten dramatisch schnell.