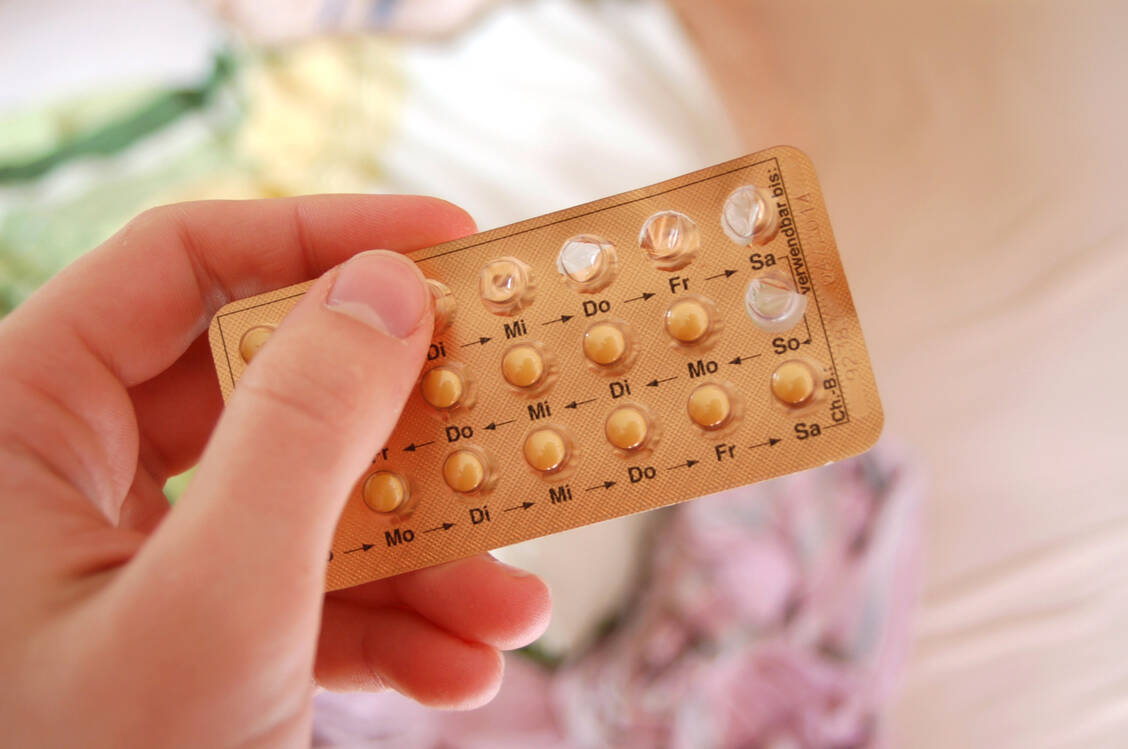
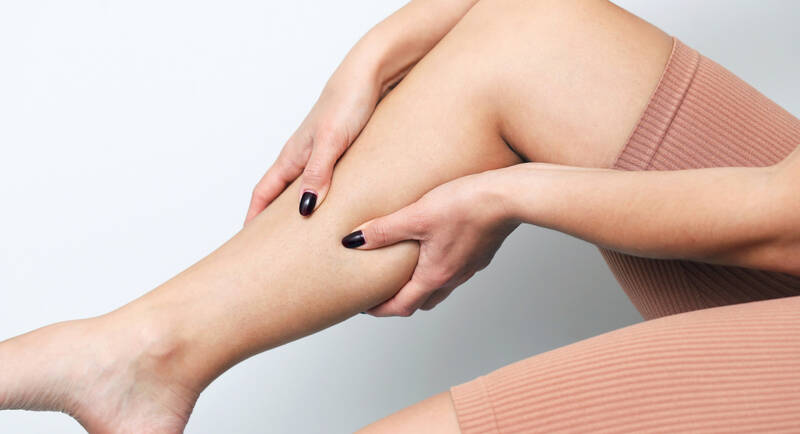
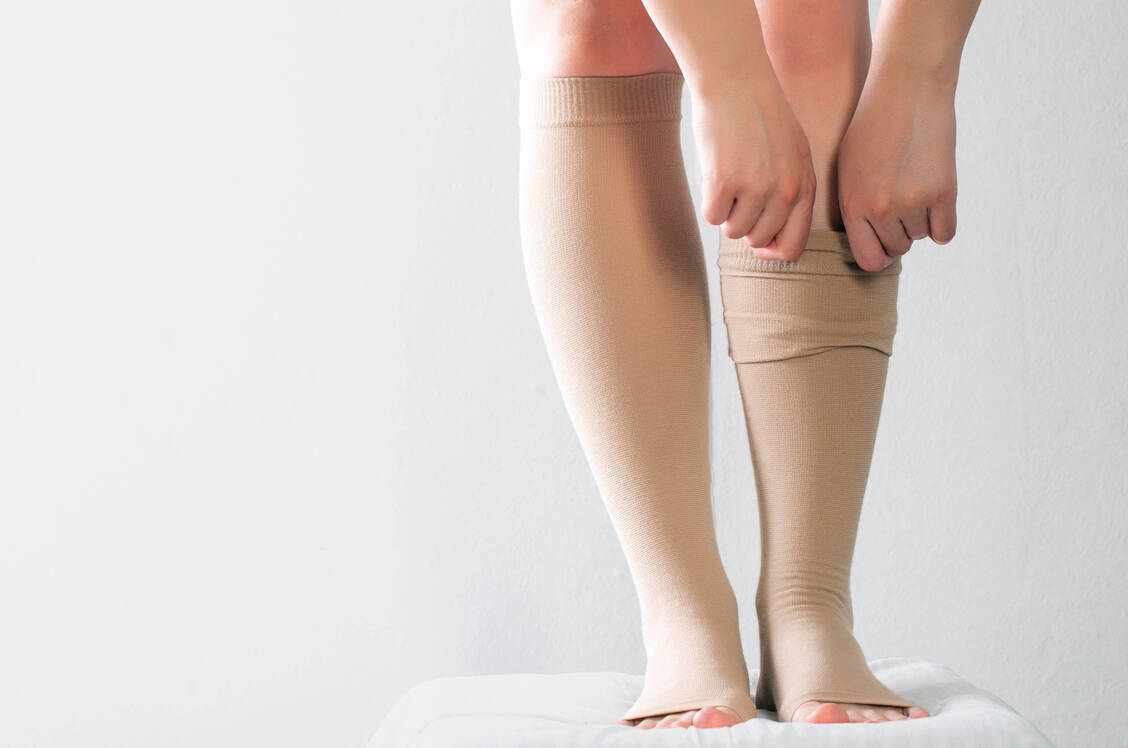
Die Risikofaktoren Immobilisation, Bewegungsmangel und extreme Hitze lassen sich gut anhand der Virchow-Trias erklären.
Bei langem Sitzen mit gebeugten Beinen wird der venöse Rückstrom behindert. Besonders in den tiefen Venen der unteren Extremitäten kommt es zu einer venösen Stase. Die Muskelpumpe der Waden, die normalerweise den venösen Rückfluss unterstützt, ist inaktiv. Dadurch steigt die Wahrscheinlichkeit, dass sich Thromben bilden.
Eine dauerhafte Druckbelastung auf die Beinvenen, zum Beispiel durch die Sitzkante, kann zu mikroskopischen Endothelschäden führen. Auch eine durch Hypoxie bedingte Dysfunktion des Endothels kann auftreten, besonders bei niedrigem Kabinendruck im Flugzeug. Ein geschädigtes Endothel wiederum exprimiert prothrombotische Faktoren.
Langstreckenreisen und extreme Hitze sind oft mit Dehydratation verbunden, zum Beispiel durch trockene Kabinenluft im Flugzeug und geringe Flüssigkeitsaufnahme. Eine verminderte Plasmavolumenfraktion erhöht die Blutviskosität.