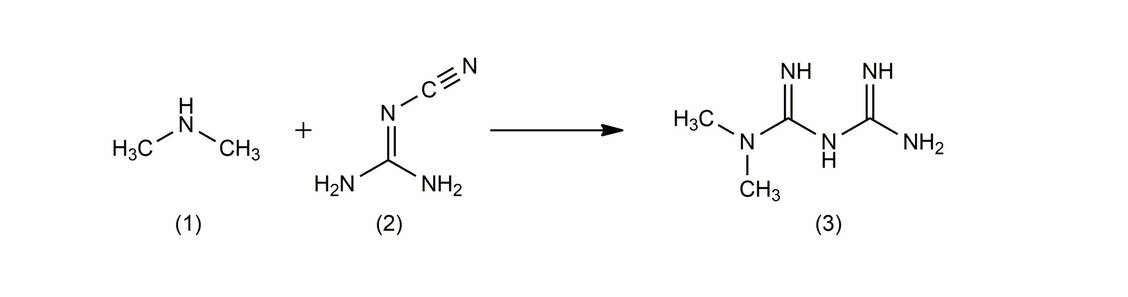
Metformin ist wegen der hohen Wirksamkeit, der niedrigen Kosten und des geringen Hypoglykämierisikos Mittel der Wahl für die Behandlung des Typ-2-Diabetes. Die Verordnungen zu Lasten der Gesetzlichen Krankenversicherung in Deutschland sind seit mehr als 20 Jahren kontinuierlich angestiegen, stagnierten von 2011 bis 2017 auf einem hohen Niveau von etwa 600 Millionen definierten Tagesdosen (DDD) und sind seitdem wieder um fast 10 Prozent gestiegen.
Die aktuellen DDD-Nettokosten liegen bei 20 Cent. Noch vor zehn Jahren lagen sie bei 30 Cent, was bedeutet, dass der Preis für diesen enorm wichtigen Arzneistoff innerhalb der letzten Dekade – nicht zuletzt wegen der Rabattverträge – um ein Drittel gesunken ist. An dieser Stelle bleibt festzuhalten, dass der Preisdruck bei Generika in Deutschland keine kausale Begründung für das Auftreten von Nitrosaminen in lebenswichtigen Arzneimitteln ist, allerdings auch kein Argument für hohe und gleichbleibende pharmazeutischen Qualität von Arzneistoffen beziehungsweise Arzneimitteln.