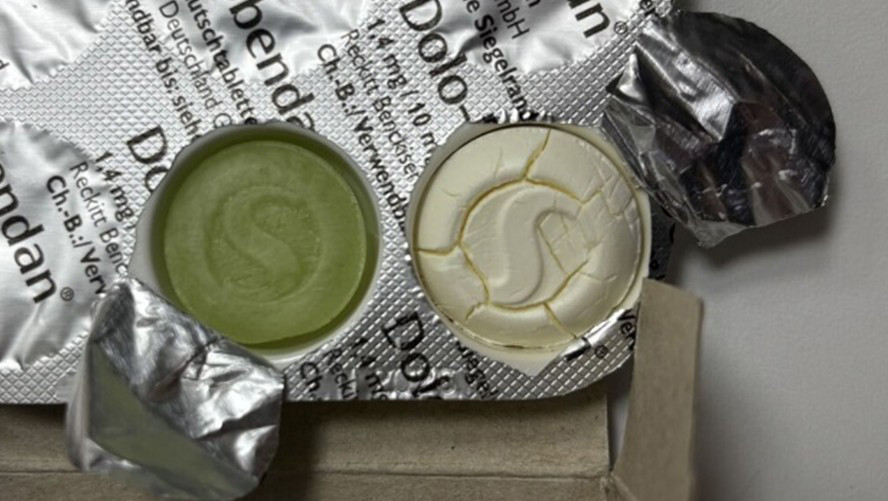
Die Weißverfärbungen wurden erst nach der Umstellung auf die zuckerfreie Rezeptur im Juli 2023 beobachtet. Seitdem ersetzt der Firma zufolge der Zuckeraustauschstoff Isomalt die ursprünglichen Hilfsstoffe Glucose und Sucrose in den Lutschtabletten. Im Zuge dessen sei auch die Beschichtung der PVC-Blisterfolie verstärkt worden, die Aluminiumfolie blieb unverändert.
Laut AMK prüft die Firma aktuell den gesamten Prozess von Rezepturentwicklung über Herstellung bis hin zu Verpackung. Die firmeneigenen Rückstellmuster der gemeldeten Chargen hätten keine weißen Veränderungen gezeigt.
Die Firma vermutet gegenüber der AMK, dass Feuchtigkeit in beschädigte Blisterzellen eingedrungen sein könnte, zum Beispiel durch Mikrorisse in der Aluminiumfolie. Diese könnten entstehen, wenn das Präparat unsachgemäß gehandhabt oder gelagert werde, zum Beispiel durch Zuschneiden der Blister oder Lagerung außerhalb des Umkartons unter feuchten Bedingungen.