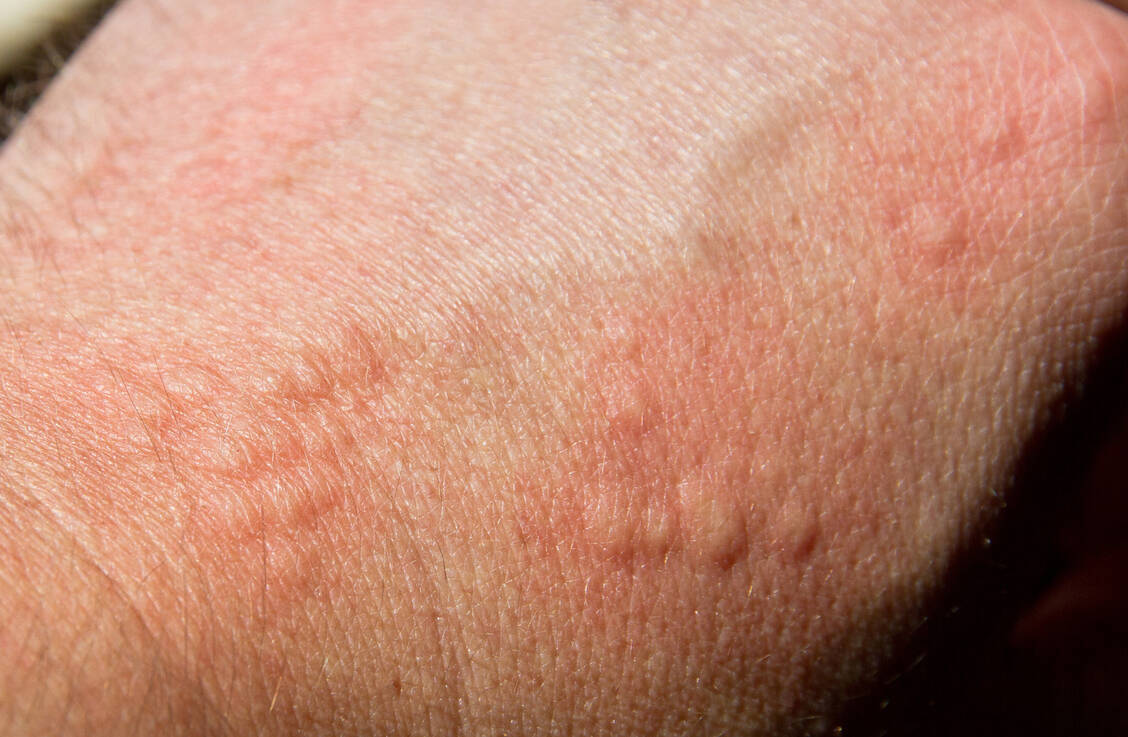
Das EMA-Gremium plädiert dafür, das Fertigarzneimittel Rhapsido® 25 mg Filmtabletten von Novartis zur Behandlung der chronisch spontanen Urtikaria bei erwachsenen Patienten, die auf eine Behandlung mit H1-Antihistaminika nicht ausreichend ansprechen, zuzulassen. Darin enthalten ist mit Remibrutinib ein bislang noch nicht auf dem deutschen Markt eingeführter Arzneistoff. Es handelt sich um einen Inhibitor des Enzyms Brutonkinase (BTK). Die Aktivierung der BTK-Signalkaskade führt bei chronisch spontaner Urtikaria zur Ausschüttung von Histamin und proinflammatorischen Mediatoren, was zur Quaddelbildung und Schwellungen führt. Durch die Blockade von BTK wird das verhindert. Remibrutinib ist ein hochselektiver, kovalenter, oral zu verabreichender BTK-Hemmer. Die in der US-Fachinformation empfohlene orale Dosierung beträgt zweimal täglich 25 mg.