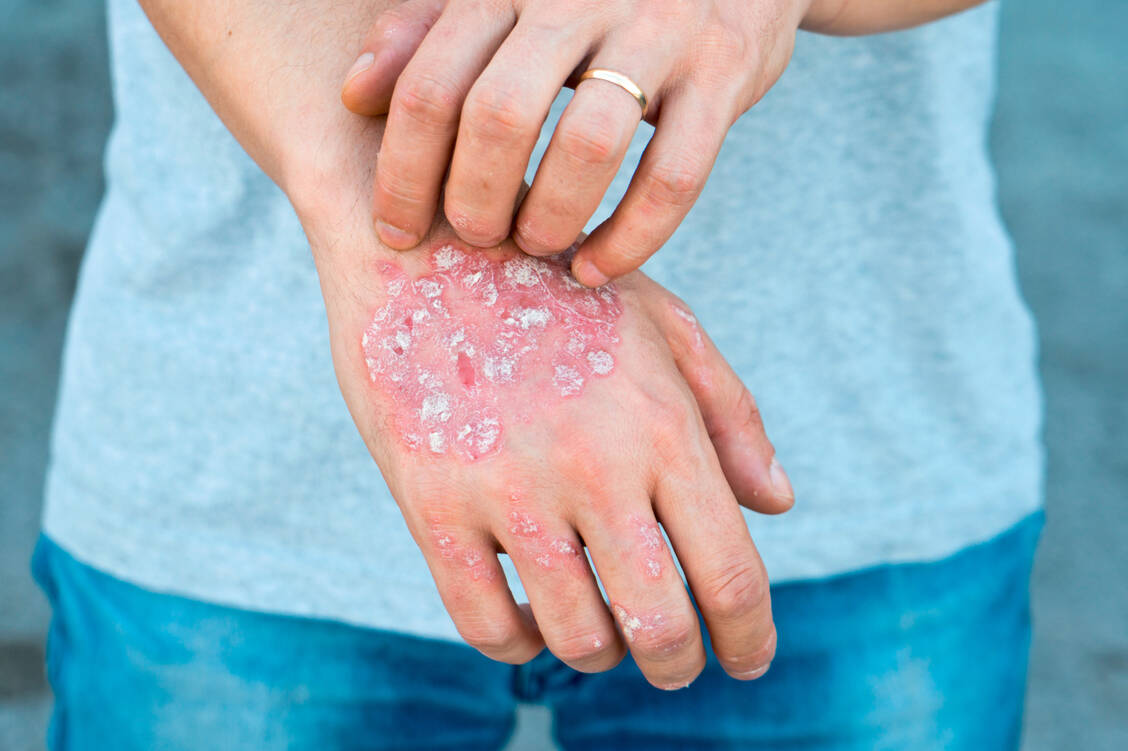
Die Zulassung stützt sich auf die Ergebnisse der drei publizierten Phase-III-Studien BE VIVID, BE READY und BE SURE, in denen die Wirksamkeit und Sicherheit von Bimekizumab bei 1480 Erwachsenen mit mittelschwerer bis schwerer Plaque-Psoriasis geprüft wurden. Die Erkrankung besserte sich unter Bimzelx stärker als unter Placebo oder den Antikörpern Ustekinumab oder Adalimumab. In den Studien sanken die PASI-Scores (als Maß für die Schwere der Psoriasis und die betroffene Hautfläche) nach 16 Wochen bei 85 bis 91 Prozent der Patienten, die Bimekizumab alle vier Wochen erhielten, um etwa 90 Prozent. Dies war bei 1 bis 5 Prozent der Patienten unter Placebo, bei der Hälfte der Patienten unter Ustekinumab und bei 47 Prozent unter Adalimumab der Fall. Nach 16 Wochen war die Haut bei 84 bis 93 Prozent der Patienten mit Bimekizumab (fast) erscheinungsfrei, verglichen mit 1 bis 5 Prozent unter Placebo, 53 Prozent unter Ustekinumab und 57 Prozent unter Adalimumab. Das mit dem Neuling erreichte klinische Ansprechen blieb über ein Jahr erhalten.