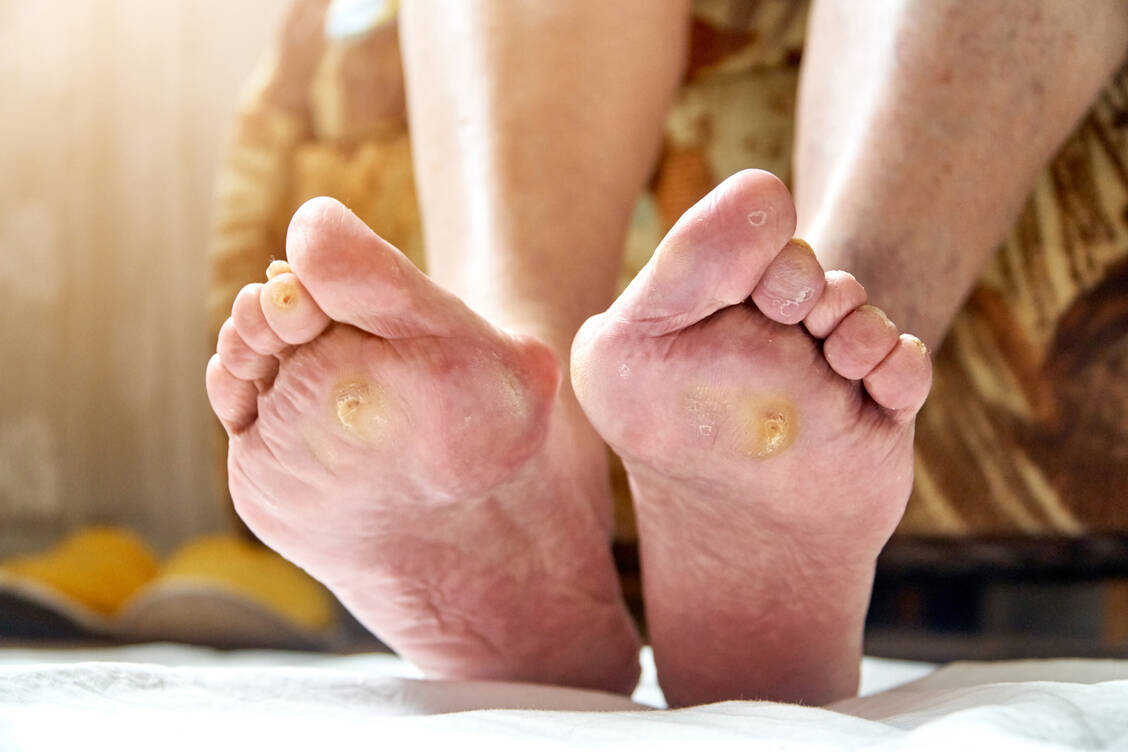
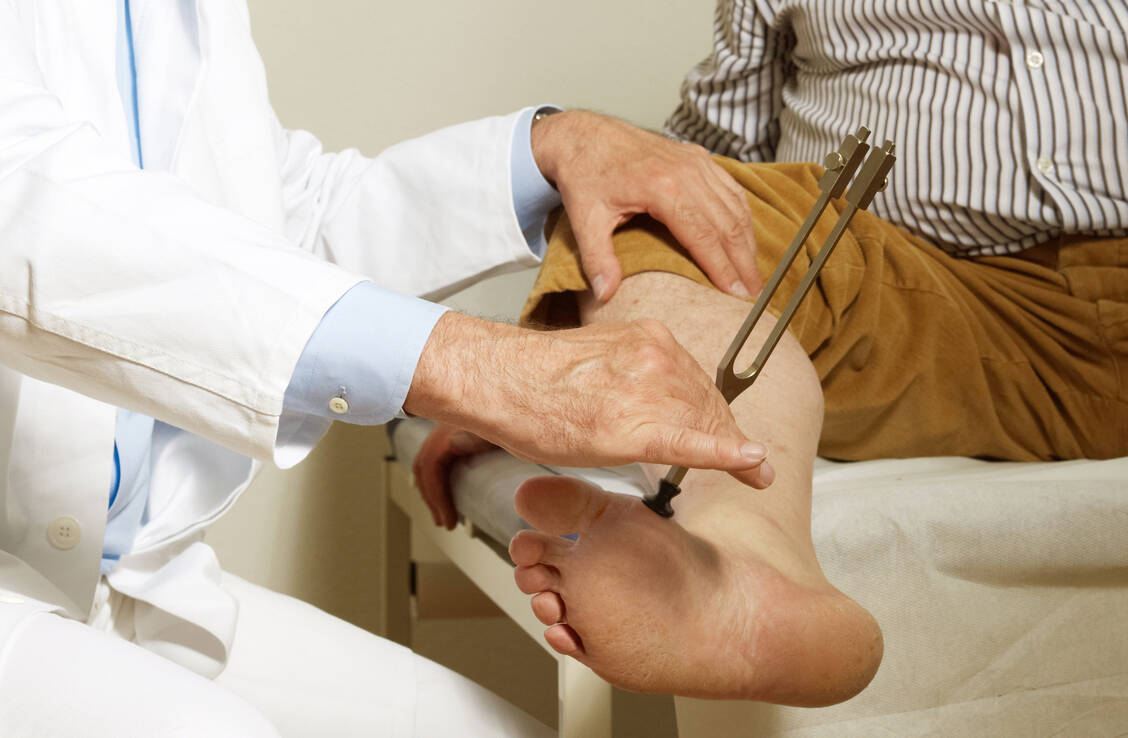
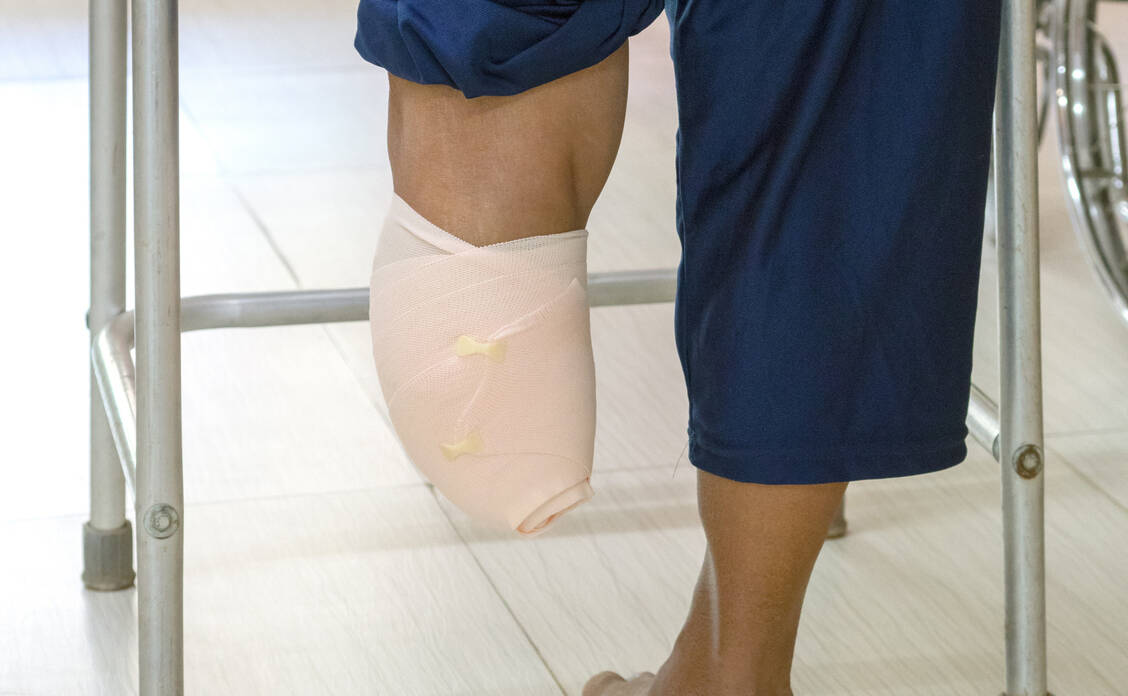
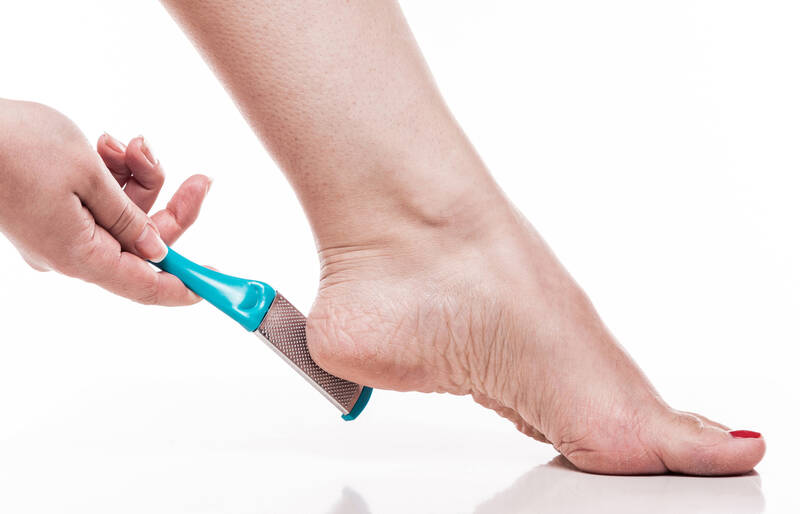
Die Fußuntersuchung sollte ein selbstverständlicher Teil der regelmäßigen Kontrollen bei Diabetes-Patienten sein. Sie umfasst die Anamnese nach Symptomen (brennende, stechende Schmerzen, Parästhesien, Taubheitsempfinden, fehlendes Empfinden), die manuelle Fußuntersuchung (auf Hautstatus, Muskulatur, eventuell Deformitäten, Beweglichkeit, Temperatur), die Prüfung der Drucksensibilität (mit 10 g Monofilamenten oder Stimmgabel) und der Fußpulse sowie weitere Untersuchungen zur Diagnose einer potenziellen pAVK, zum Beispiel Dopplersonografie, farbkodierte Duplexsonografie und Angiografie.
Ein diagnostiziertes DFS wird nach Ausmaß und Ursachen weiter klassifiziert. Durchgesetzt hat sich die kombinierte Wagner-Armstrong-Klassifikation (Tabelle 3). Ebenfalls weit verbreitet ist die PEDIS-Klassifikation, die von der International Working Group on the Diabetic Foot (IWGDF) 2003/2004 erarbeitet wurde (3). Der Begriff »Pedis« ist nicht nur vom Lateinischen (pes: Fuß, Genitiv Singular pedis) abgeleitet, sondern klassiert die Faktoren rund um das DFS: