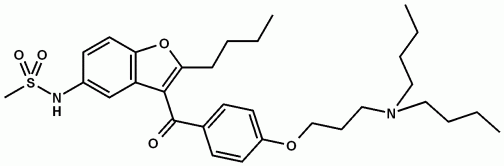
Die Liste der möglichen Wechselwirkungen ist lang, da Dronedaron hauptsächlich über das Cytochrom-Isoenzym CYP-3A4 metabolisiert wird und seinerseits die CYP-Enzyme 3A4 und 2D6 sowie den Arzneimitteltransporter P-Glykoprotein (P-gp) hemmt. Die gleichzeitige Anwendung von starken CYP-3A4-Inhibitoren wie Ketoconazol und anderen Azolen, Telithromycin, Nefazodon und Ritonavir ist kontraindiziert, da die Dronedaron-Konzentration im Blut erheblich steigen kann. Daher ist auch Grapefruitsaft zu meiden. Mäßig starke Inhibitoren wie Calciumantagonisten können die Dronedaron-Exposition ebenfalls erhöhen; in klinischen Studien wurde aber kein erhöhtes Risiko für Blutdruckabfall, Bradykardie oder Herzsuffizienz beobachtet. Der Patient sollte zudem die gleichzeitige Einnahme von potenten CYP-3A4-Induktoren wie Phenobarbital, Carbamazepin, Phenytoin und Johanniskraut meiden, da diese den Abbau von Dronedaron ankurbeln.
Dronedaron seinerseits kann den Abbau von Arzneistoffen, die über CYP-3A4 und -2D6 metabolisiert werden, verlangsamen. Dies gilt beispielsweise für Statine, Sirolimus und Tacrolimus sowie Betablocker. Die Dosis von Digitalis soll bei gleichzeitiger Gabe halbiert werden, da Dronedaron die Herzglykosidspiegel erhöhen kann.