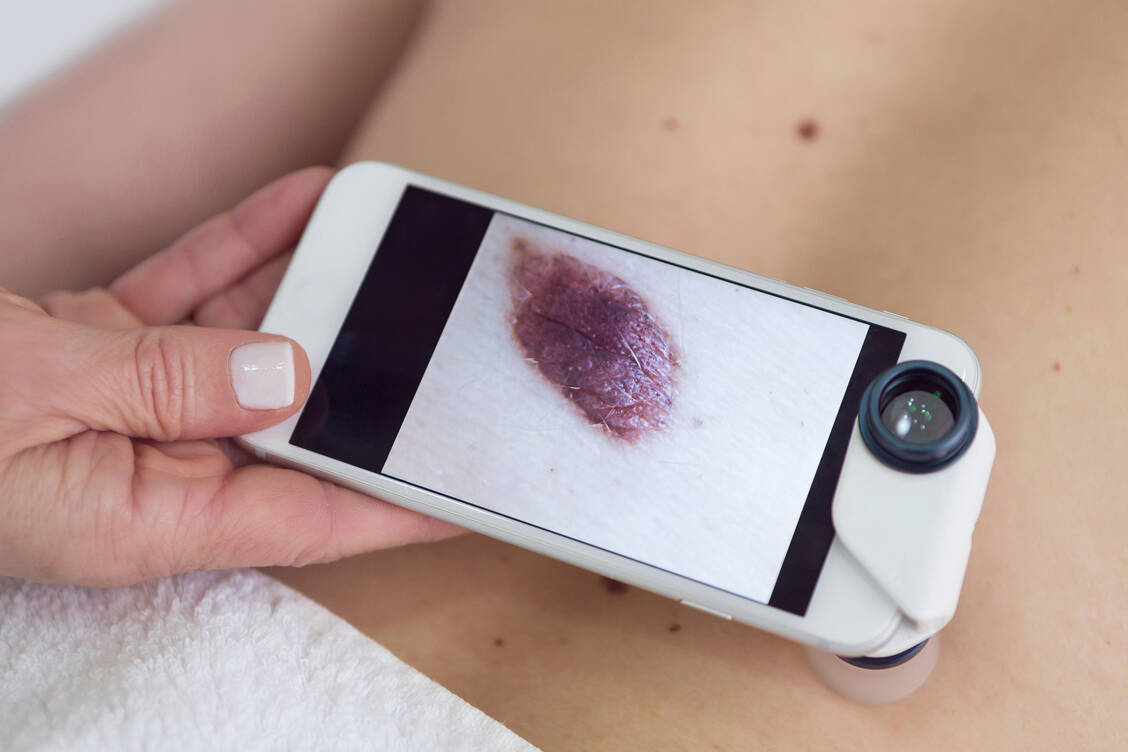
Zwar haben einer Analyse in 39 Ländern zufolge etwa 10 bis 30 Prozent der Ärzte KI-Anwendungen schon einmal verwendet (»Frontiers in Medicine« 2022, DOI: 10.3389/fmed.2022.990604). Jedoch mangelt es vielen Medizinern an Vertrauen in die Zuverlässigkeit der Systeme. So gebe es nur wenige Studien, die die Wirksamkeit der KI-Anwendungen zeigen, betonen Rajpurkar und Lungren. Zudem seien die KI-Anwendungen häufig nicht außerhalb des Umfelds getestet, in dem sie trainiert wurden – nicht einmal die Systeme mit FDA-Zulassung. Es sei daher schlecht abzuschätzen, wie gut die Übertragbarkeit auf andere klinische Umgebungen mit anderen Patientengruppen und leicht unterschiedlichen Bildgebungsprozessen, zum Beispiel unterschiedliche Gerätehersteller von MRT- oder Röntgengeräten in verschiedenen Krankenhäusern, ist.