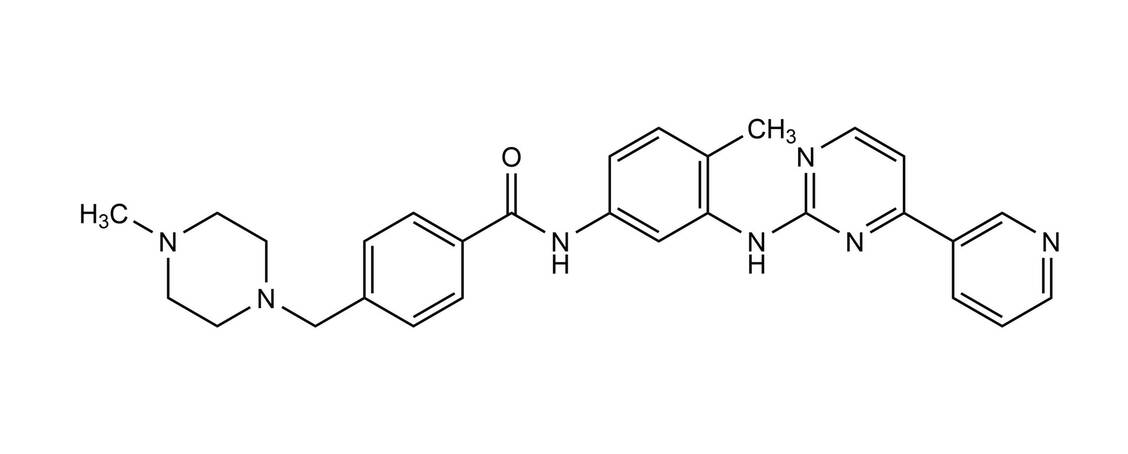
Die erste Indikation war die Philadelphia-Chromosom-positive (Ph+) CML. Imatinib wird bei Erwachsenen und Kindern mit neu diagnostizierter Ph+ CML angewendet, für die eine Knochenmarktransplantation nicht infrage kommt. Zudem wird es bei Erwachsenen und Kindern in der chronischen Phase der Krankheit eingesetzt, wenn diese auf Interferon α nicht ansprechen, sowie in der akzelerierten Phase und der Blastenkrise.
In Kombination mit einer Chemotherapie wird Imatinib auch bei Erwachsenen und Kindern mit neu diagnostizierter Ph+ akuter lymphatischer Leukämie (ALL) angewendet. Bei Erwachsenen mit rezidivierter oder refraktärer Ph+ ALL ist es als Monotherapie zugelassen.
Imatinib darf auch bei Erwachsenen mit myelodysplastischen/myeloproliferativen Erkrankungen (MDS/MPD) in Verbindung mit Genumlagerungen des PDGF-Rezeptors zum Einsatz kommen. Ebenso ist es bei Erwachsenen mit fortgeschrittenem hypereosinophilem Syndrom (HES) und/oder chronischer eosinophiler Leukämie (CEL) mit FIP1L1-PDGFRα-Umlagerung zugelassen.
Ein weiteres Einsatzgebiet von Imatinib ist die Behandlung von c-Kit-(CD117)-positiven nicht resezierbaren und/oder metastasierten malignen gastrointestinalen Stromatumoren (GIST) bei Erwachsenen und die adjuvante Behandlung Erwachsener mit signifikantem Risiko eines Rezidivs nach Resektion c-Kit-(CD117)-positiver GIST.
Schließlich ist der Tyrosinkinase-Hemmer zugelassen zur Behandlung Erwachsener mit nicht resezierbarem Dermatofibrosarcoma protuberans (DFSP) und Erwachsener mit rezidivierendem und/oder metastasiertem DFSP, die für eine chirurgische Behandlung nicht infrage kommen.