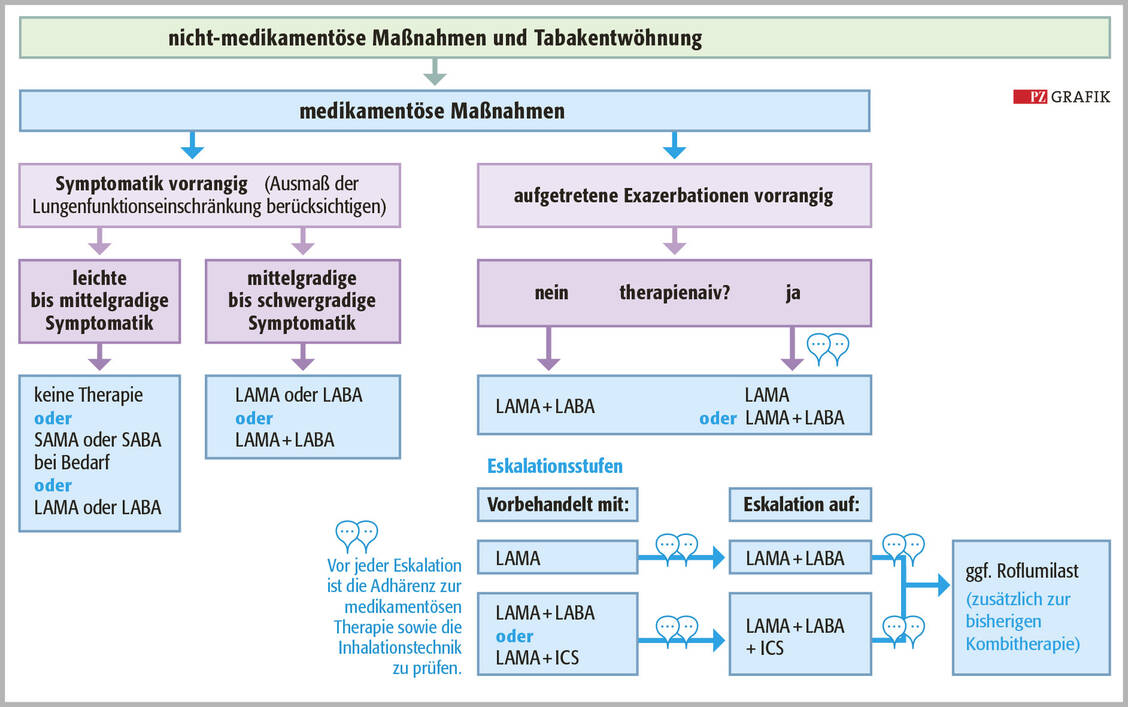
Elektrische Vernebler erzeugen das Aerosol passiv durch Druckluft oder Ultraschall, sind ebenfalls unabhängig von der Mitarbeit des Patienten und funktionieren auch bei geringem Einatemfluss. Die Medikamentenapplikation kann durch Aufsätze mit einer Stenose-Atmung kombiniert werden.
Die aktive Aerosolerzeugung aus Pulverinhalatoren erfordert Energie, die in unterschiedlichem Ausmaß durch den Druckabfall im Pulverinhalator oder durch die Scherkräfte einer forcierten Einatmung generiert wird.
Für viele Patienten, aber auch für viele Ärzte sind die erforderlichen Atemzugmanöver und deren Folgen für die bronchiale Deposition nicht recht nachvollziehbar. Hier hilft die Fachkompetenz von Apothekern weiter, die den Patienten entsprechend instruieren können.
Prinzipiell gilt: Je kleiner die Aerosolteilchen sind, desto langsamer und länger soll eingeatmet werden, um den Teilchen Gelegenheit zur Sedimentation im Bronchialbaum zu geben. Das gilt für Dosieraerosole, Sprühvernebler und elektrische Vernebler; die inspiratorische Anstrengung ist dabei gering. Das Atemmanöver beginnt mit tiefer Ausatmung (Exspiration), anschließend langsamer maximaler Einatmung (Inspiration) und endet mit einer langsamen Exspiration gegen die Lippenbremse.