Die EU-Kommission hat Novartis die Zulassung für den monoklonalen Antikörper Erenumab (Aimovig®) erteilt. Indiziert ist das Präparat zur Migräne-Prophylaxe für erwachsene Patienten, die an mindestens vier Tagen im Monat unter Migräne leiden. Es ist das erste Medikament, das speziell zur Vorbeugung von Migräneattacken entwickelt wurde. Verschreiben sollen das neue Medikament nur Ärzte, die mit der Diagnose und Behandlung von Migräne Erfahrung haben.
Die Injektionslösung mit 70 mg Erenumab kommt als Fertigspritze und Fertigpen auf den Markt. Die Patienten können sich das Mittel alle vier Wochen selbst subkutan in den Oberschenkel oder den Bauch injizieren. Wenn nötig, ist auch eine monatliche Dosis von 140 mg Erenumab möglich.
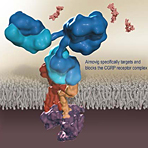
Erenumab blockt spezifisch den Calcitonin Gene-related Peptide (CGRP)-Rezeptor. CGRP ist ein Neuropeptid, das vermutlich die Schmerzsignale bei Migräneattacken weiterleitet und gefäßerweiternd wirkt. Beim Beginn einer Attacke sind die CGRP-Spiegel erhöht und wieder auf Normalniveau, wenn die Attacke beendet ist. Infundiert man Probanden CGRP, löst dies migräneähnliche Kopfschmerzen aus.
Im Studienprogramm mit rund 2600 Teilnehmern trat bei der Mehrheit der Patienten, die auf die Therapie ansprachen, ein Schutzeffekt vor Migräneattacken innerhalb von drei Monaten auf. Bei Patienten, die nach drei Monaten Behandlung nicht ansprechen, sollte erwogen werden, die Behandlung abzusetzen, heißt es in der Zusammenfassung des Arzneimittels. In regelmäßigen Abständen soll evaluiert werden, ob die Behandlung weiter anschlägt.
Bei Patienten mit chronischer Migräne (im Schnitt 18 Tage pro Monat) und die bereits erfolglos mit anderen Medikamenten prophylaktisch behandelt wurden, sank die Zahl der Migränetage je nach Dosis und Vorbehandlung um 2,5 bis 4,3 Tage. 34,7 Prozent erreichten unter 70 mg Erenumab eine Reduktion um mindestens 50 Prozent gegenüber 17,3 Prozent unter Placebo. Auch bei Patienten mit episodischer Migräne (im Schnitt acht Tage pro Monat) zeigte sich eine Schutzwirkung. Sie litten unter 140 mg Erenumab 2,5 Tage und unter 70 mg Erenumab 2,0 Tage weniger unter Migränekopfschmerz als die Patienten der Placebogruppe. Als Nebenwirkung traten häufig Verstopfung, Juckreiz, Muskelspasmen und Reaktionen an der Einstichstelle auf. Zu den häufigsten Nebenwirkungen zählen zudem virale Infekte der oberen Atemwege, Sinusitis, Influenza und Rückenschmerzen.
Novartis will das Medikament im November in Deutschland auf den Markt bringen. Um Aimovig den Patienten schnellstmöglich zur Verfügung zu stellen, strebe Novartis zunächst eine Erstattung auf Basis der vorhandenen Evidenz an, die im AMNOG-Prozess akzeptiert wird, teilte die deutsche Niederlassung mit. Dies seien die schwer betroffenen Patienten. Parallel werde für die leichter betroffenen Patienten geeignete Evidenz generiert und dem G-BA zeitnah nach Studienabschluss zur Bewertung vorgelegt. (dh)
31.07.2018 l PZ
Foto: Novartis



