
Weitere Angebote der PZ

© 2025 Avoxa - Mediengruppe Deutscher Apotheker GmbH
Sufentanil: EU-Zulassung für neuartiges Applikationssystem |
Die EU-Kommission hat das innovative Applikationssystem Zalviso zur Behandlung von starken postoperativen Schmerzen zugelassen. Darüber informiert Hersteller Grünenthal in einer Pressemitteilung. Das tragbare, nicht-invasive System ermöglicht es erwachsenen Patienten im Krankenhaus, sich selbst, je nach individuellem Bedarf, mit sublingualem Sufentanil zu behandeln. Die Wirkung soll vergleichbar schnell einsetzen wie nach intravenöser Verabreichung des Opioids.
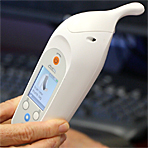
Die Zulassung Zalviso® basiert auf den Daten einer klinischen Phase-III-Studie. Nach Ansicht der Patienten, die sich einem großen Gelenkersatz oder einer offenen Bauch-OP unterzogen hatten, schnitt sublinguales Sufentanil im Vergleich zu intravenösem Morphin besser ab. Das elektronisch programmierte Applikationsgerät (Foto) gibt eine individuelle Dosis Sufentanil in Form von 15 μg Nano-Tabletten ab, die der Patient bei Bedarf per Knopfdruck anfordert. Dabei wird das Mundstück unter die Zunge platziert. Damit es trotz der Steuerung durch den Patienten nicht zu einer Überdosierung kommt, ist zwischen zwei Applikationen eine 20-minütige Sperrzeit eingebaut. Das Opioid wird in einer Kartusche mit 40 Sufentanil-Nano-Tabletten geliefert. Diese Menge ist ausreichend für zwei bis drei Tage, die durchschnittliche Dauer einer postoperativen Schmerzbehandlung.
Sufentanil ist ein starkes Opioid (sieben- bis zehnfach potenter als Fentanyl) und das derzeit stärkste zugelassene Schmerzmittel. Bisher ist es nur in Form einer Injektionslösung verfügbar. Laut Grünenthal soll Zalviso ab der ersten Hälfte 2016 auf dem Markt verfügbar sein. (rt)
29.09.2015 l PZ
Foto: Acel Rx Pharmaceuticals